|
تضامنًا مع حق الشعب الفلسطيني |
ليزوفوسفاتيديل-كولين
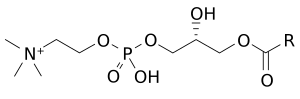
ليزوفوسفاتيديل كولين (بالإنجليزية: Lysophosphatidylcholine)(LPC ،lysoPC)، وتسمى أيضًا ليزوليسيثين وهي فئة من المركبات الكيميائية المشتقة من فوسفاتيديل كولين.[1]
نظرة عامة
يُنتج ليزوفوسفاتيديل كولين عن طريق عملية التحلل المائي الجزئي لفوسفاتيديل كولين والتي يتم فيها إزالة إحدى مجموعات الأحماض الدهنية، يكون التحلل المائي بشكل عام نتيجة لعمل إنزيم الفوسفوليباز A2.[2] ومن خصائص الليزوفوسفاتيديل كولين أنه ينشط الخلايا البطانية أثناء تصلب الشرايين المبكر[3][4] ويحفز دفاع الخلايا البلعمية عندما تطلقها الخلايا الاستماتية،[5] يمكن أيضا استخدام LPC في المختبر ليقوم بإزالة الميالين من شرائح الدماغ لتقليد آثار أمراض إزالة الميالين مثل التصلب المتعدد، ومن المعروف أنه يحفز الخلايا البلعمية من غلاف الميالين ويمكن أن يغير الخصائص السطحية لخلايا الدم الحمراء،[6] يُعتقد أن إزالة الميالين الناجم عن LPC تحدث من خلال إجراءات الخلايا البلعمية والخلايا الدبقية الصغيرة التي تُرى البلعم القريب من الميالين، ويعتقد أيضًا أن الخلايا التائية الغازية تتوسط في هذه العملية، تستخدم البكتيريا مثل «الفيلقية المستروحة» المنتجات النهائية من فوسفوليبيز A2 (الأحماض الدهنية و ليزوفوسفوليبيد) لتسبب موت الخلايا العائلة (البلاعم) من خلال إطلاق السيتوكروم C.
يوجد LPC على شكل فوسفوليبيدات ثانوية في غشاء الخلية (≤ 3٪) وفي بلازما الدم (8-12٪). نظرًا لأن LPC يتم استقلابه بسرعة عن طريق ليزوفوسفوليبز وأسيل ترانسفيرز-LPC فإنه يدوم لفترة قصيرة فقط في الجسم الحي، من خلال استبدال مجموعة أسيل داخل LPC بمجموعة ألكيل تم تصنيع ألكيل-ليزوفوسفولبييد (ALP)، نظائر LPC مستقرة في عملية الأيض ومنها ماهو تحت البحث والتطوير مثل إديلفوسين وميلتيفوسين وبيريفوسين وذلك لكي تستخدم كأدوية ضد السرطان وأمراض أخرى،[6][7] اُكتشِف أن معالجة ليزوفوسفاتيديل كولين هي عنصر أساسي لتطور الدماغ البشري الطبيعي: أولئك الذين ولدوا بجينات تمنع الامتصاص الكافي يعانون من صغر الرأس المميت.[8]
يحدث LPC في العديد من الأطعمة بشكل طبيعي، في النشا: الطبعة الثالثة للكيمياء والتكنولوجيا في الصفحة 592 ذكر المؤلفون أن ليزوفوسفاتيديل كولين يشكل حوالي 70% من الدهون في نشا الشوفان.[9]
تُعتبر القدرات المضادة للسرطان لمتغيرات LPC الاصطناعية خاصة لأنها لا تستهدف الحمض النووي للخلية ولكنها تدخل في غشاء البلازما وتسبب موت الخلايا المبرمج من خلال التأثير على العديد من مسارات الإشارة، لذلك تكون آثارها مستقلة عن حالة تكاثر الخلية السرطانية.[10]
التطبيقات الصناعية للإنزيمات التي تُنتج الليزوفوسفاتيديل كولين
إن زيت فودبرو ليزوماكسا هو مستحضر إنزيم الفوسفوليباز A2 التجاري المعتمد من قِبل إدارة الأغذية والعقاقير والذي يُستخدم لإزالة تكسير الزيوت النباتية في المنتجات على نطاق واسع لزيادة المحصول، تُعد الأشكال المختلفة من ليزوفوسفاتيديل كولين هي المنتجات الرئيسية لهذا الإنزيم،[11] تمت دراسة ليزوفوسفاتيديل كولين كمنشط مناعي لتمييز الخلايا الأحادية إلى الخلايا التغصنية الناضجة،[12] يضخم ليزوفوسفاتيديل كولين الموجود في الدم جينات TLR الميكروبية التي تسببها الاستجابات الالتهابية من الخلايا البشرية مثل الخلايا الظهارية المعوية والبلاعم/الوحيدات.[13] وهذا له تأثير على تعفن الدم الناجم عن الميكروبات.
التركيب في الأطعمة
يمثل ليزوفوسفاتيديل كولين نسبة 4.6% من الدهون الفوسفاتية الموجودة في زيت جوز الهند والتي تشكل 0.2% من الدهون في زيت جوز الهند، هذا مقارنة بالزيوت النباتية التي قد تحتوي على 2-3% فوسفوليبيدات.[14]
ليزوفوسفاتيديل كولين وتصلب الشرايين
تمت دراسة سمك بطانة الشريان لدي بعض المدخنين الشباب حيث يرتبط هذا السمك بشكل إيجابي مع انخفاض تدفق الدم، أشارت الأدلة إلى التدخين كعامل خطر رئيسي لزيادة مستويات إنزيم الفوسفوليباز A2 بسبب تأثير دخان التبغ على أكسدة جزيئات LDL المحتفظ بها في الجزء الداخلي من الشريان السباتي.[15] مما قد يكون له تأثير ضار على الصحة العامة.
المراجع
- ^ "Lysophospholipids induce innate immune transdifferentiation of endothelial cells, resulting in prolonged endothelial activation". The Journal of Biological Chemistry. ج. 293 ع. 28: 11033–11045. مايو 2018. DOI:10.1074/jbc.RA118.002752. PMID:29769317.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ Phosphatidylcholine and related lipids نسخة محفوظة 2009-05-31 على موقع واي باك مشين., lipidlibrary.co.uk
- ^ "Mitochondrial Reactive Oxygen Species Mediate Lysophosphatidylcholine-Induced Endothelial Cell Activation". Arteriosclerosis, Thrombosis, and Vascular Biology. ج. 36 ع. 6: 1090–100. أبريل 2016. DOI:10.1161/ATVBAHA.115.306964. PMID:27127201.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "IL-35 (Interleukin-35) Suppresses Endothelial Cell Activation by Inhibiting Mitochondrial Reactive Oxygen Species-Mediated Site-Specific Acetylation of H3K14 (Histone 3 Lysine 14)". Arteriosclerosis, Thrombosis, and Vascular Biology. ج. 38 ع. 3: 599–609. مارس 2018. DOI:10.1161/ATVBAHA.117.310626. PMID:29371247.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ Lauber، K؛ Bohn, E؛ Kröber, SM؛ Xiao, Y (2003). "Apoptotic Cells Induce Migration of Phagocytes via Caspase-3-Mediated Release of a Lipid Attraction Signal". Cell. ج. 113 ع. 6: 717–730. DOI:10.1016/S0092-8674(03)00422-7. PMID:12809603.
- ^ أ ب Munder، PG؛ Modolell M؛ Andreesen R؛ Weltzien HU؛ Westphal O (1979). "Lysophosphatidylcholine (Lysolecithin) and its Synthetic Analogues. Immunemodulating and Other Biologic Effects". Springer Seminars in Immunopathology. ج. 203 ع. 2: 187–203. DOI:10.1007/bf01891668.
- ^ Houlihan، W؛ Lohmeyer M؛ Workman P؛ Cheon SH (1995). "Phospholipid antitumor agents". Medicinal Research Reviews. ج. 15 ع. 3: 157–223. DOI:10.1002/med.2610150302. PMID:7658750.
- ^ Guemez-Gamboa، Alicia؛ N Nguyen؛ Hongbo Yan (2015). "Inactivating mutations in MFSD2A, required for omega-3 fatty acid transport in brain, cause a lethal microcephaly syndrome". Nature Genetics. ج. 47 ع. 7: 809–813. DOI:10.1038/ng.3311. PMID:26005868.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ Bemiller، James N.؛ Whistler، Roy L. (6 أبريل 2009). Starch. ISBN:9780080926551. مؤرشف من الأصل في 2020-07-31.
- ^ van Blitterswijk، W؛ Verheij M (2008). "Anticancer alkylphospholipids: mechanisms of action, cellular sensitivity and resistance, and clinical prospects". Current Pharmaceutical Design. ج. 14 ع. 21: 2061–74. DOI:10.2174/138161208785294636. PMID:18691116.
- ^ Michael Eskin، N. A.؛ Shahidi، Fereidoon (8 أكتوبر 2012). Biochemistry of Foods. ISBN:9780080918099. مؤرشف من الأصل في 2020-07-31.
- ^ "Patent US20110135684 - Use of L-alpha-lysophosphatidylcholine to obtain the differentiation of... - Google Patents". google.com.mx. مؤرشف من الأصل في 2020-07-31.
- ^ Sharma, Naveen; Akhade, Ajay Suresh; Ismaeel, Sana; Qadri, Ayub. "Serum-borne lipids amplify TLR-activated inflammatory responses". Journal of Leukocyte Biology (بEnglish). n/a (n/a). DOI:10.1002/JLB.3AB0720-241RR. ISSN:1938-3673. Archived from the original on 2020-07-30.
- ^ "Rahman's page 12 chart" (PDF). مؤرشف من الأصل (PDF) في 2014-03-28. اطلع عليه بتاريخ أكتوبر 2020.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - ^ Fratta Pasini، A؛ Stranieri، C؛ Pasini، A؛ Vallerio، P؛ Mozzini، C؛ Solani، E؛ Cominacini، M؛ Cominacini، L؛ Garbin، U (2013). "Lysophosphatidylcholine and Carotid Intima-Media Thickness in Young Smokers: A Role for Oxidized LDL-Induced Expression of PBMC Lipoprotein-Associated Phospholipase A2?". PLOS ONE. ج. 8 ع. 12: e83092. DOI:10.1371/journal.pone.0083092. PMID:24358251.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة)