|
تضامنًا مع حق الشعب الفلسطيني |
كلوريد خماسي فلوريد الكبريت
| كلوريد خماسي فلوريد الكبريت | |
|---|---|
 |
 |
| أسماء أخرى | |
Sulfur chloride pentafluoride |
|
| الخواص | |
| الصيغة الجزيئية | SClF5 |
| الكتلة المولية | 162.51 غ/مول |
| المظهر | غاز عديم اللون |
| الكثافة | 1.54 غ/سم3 |
| نقطة الانصهار | −64 °س |
| نقطة الغليان | −17 °س |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
كلوريد خماسي فلوريد الكبريت هو مركب كيميائي لاعضوي من الهاليدات المختلطة صيغته SClF5، ويوجد في الشروط القياسية على شكل غاز عديم اللون.[1]
التحضير
يحضر المركب من تفاعل رباعي فلوريد الكبريت مع الكلور وبوجود فلوريد البوتاسيوم،[2] أو فلوريد السيزيوم عند 175 °س:[1]
كما يمكن أن تتم عملية التحضير من تفاعل رباعي فلوريد الكبريت مع أحادي فلوريد الكلور عند الدرجة 380° س:[3]
الخواص
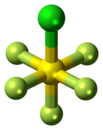
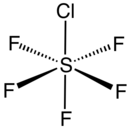
يوجد المركب في الشروط القياسية على شكل غاز عديم اللون، وهو شديد السمية؛[4] وهو يتبع بنية جزيئية ثمانية السطوح.
يتفكك المركب بالتسخين لدرجات حرارة فوق 400° س:[3]
يؤدي التفاعل مع الهيدروجين إلى الحصول على عشاري فلوريد ثنائي الكبريت:[3]
الاستخدامات
يعد كلوريد خماسي فلوريد الكبريت المركب الوحيد الذي بمكن منه إضافة مجموعة SF5 إلى المركبات العضوية.[5] من الأمثلة على ذلك:
طالع أيضاً
مراجع
- ^ أ ب Georg Brauer, unter Mitarbeit von Marianne Baudler u. a. (Hrsg.): Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I. Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 186
- ^ Leo A. Paquette: Handbook of Reagents for Organic Synthesis, Sulfur-Containing Reagents. John Wiley & Sons, 2013, ISBN 978-1-118-63483-7, S. 426
- ^ أ ب ت Ralf Steudel: Chemie der Nichtmetalle: Von Struktur und Bindung zur Anwendung. Walter de Gruyter, 2008, ISBN 3-11-021128-9, S. 565
- ^ Nyman, F., Roberts, H. L., Seaton, T. "Sulfur Chloride Pentafluoride" Inorganic Syntheses, 1966, Volume 8, p. 160. دُوِي:10.1002/9780470132395.ch42
- ^ Dolbier, William R.؛ وآخرون (2006). "A convenient and efficient method for incorporation of pentafluorosulfanyl (SF5) substituents into aliphatic compounds". Journal of Fluorine Chemistry. ج. 127: 1302–10. DOI:10.1016/j.jfluchem.2006.05.003.
| كلوريد خماسي فلوريد الكبريت في المشاريع الشقيقة: | |