|
تضامنًا مع حق الشعب الفلسطيني |
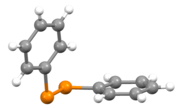
ثنائي كبريتيد ثنائي الفينيل
| ثنائي كبريتيد ثنائي الفينيل | |
|---|---|
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
1,1'-Disulfanediyldibenzene |
|
| أسماء أخرى | |
Disulfanyldibenzene |
|
| الخواص | |
| الصيغة الجزيئية | C12H10S2 |
| الكتلة المولية | 218.33 غ/مول |
| المظهر | بلورات عديمة اللون |
| نقطة الانصهار | 61-62 °س |
| الذوبانية في الماء | غير منحل |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
ثنائي كبريتيد ثنائي الفينيل هو مركب كبريت عضوي صيغته C6H5S)2)، ويوجد على شكل صلب بلوري عديم اللون. يرمز له Ph2S2، وهو واحد من أكثر مركبات ثنائي الكبريتيد العضوية المصادفة.
التحضير
يحضر المركب من أكسدة ثيوفينول بمؤكسد لطيف مثل اليود:
كما يمكن أن يستخدم بيروكسيد الهيدروجين مؤكسداً.[1]
الخواص
يوجد المركب في الشروط القياسية على شكل صلب بلوري عديم اللون، وهو لا ينحل في الماء؛ ولكنه ينحل في ثنائي إيثيل الإيثر والبنزين وثنائي كبريتيد الكربون ورباعي هيدرو الفوران.
كما هو الحال مع مركبات ثنائي الكبريتيد العضوية الحاوية على مركز C2S2 فإن Ph2S2 ليس مستوياً، وتبلغ زاوية ثنائية السطح مقدار 85°.[2]
الاستخدامات
يستخدم هذا المركب بشكل رئيسي في الاصطناع العضوي لتحضير مستبدلات فينيل الكبريت.[3]
كما يمكن أن يستخدم حفازاً لتفاعلات التصاوغ الهندسي مقرون-مفروق (cis-trans) في الألكينات تحت إشعاع من الأشعة فوق البنفسجية.[4]
طالع أيضاً
مراجع
- ^ Ravikumar,K. S.; Kesavan, V.; Crousse, B.; Bonnet-Delpon, D.; Bégué, J.-P.(2003)."Mild and Selective Oxidation of Sulfur Compounds in Trifluoroethanol: Diphenyl Disulfide and Methyl Phenyl Sulfoxide". Org. Synth.80: 184.
- ^ T.Shimizu؛ H.Isono؛ M.Yasui؛ F. Iwasaki؛ N. Kamigata (2001). "Solid State Optical Activity of Dichalcogenides: Isolation by Chiral Crystallization and Determination of Absolute Configuration". Org. Lett. ج. 3: 3639. DOI:10.1021/ol010172g.
- ^ Byers, J. H. "Diphenyl Disulfide" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. دُوِي:10.1002/047084289.
- ^ Thalmann, A. Oertle, K.; Gerlach, H.(1990)."Ricinelaidic Acid Lactone". Org. Synth.; Coll. Vol. 7: 470.
| ثنائي كبريتيد ثنائي الفينيل في المشاريع الشقيقة: | |