|
تضامنًا مع حق الشعب الفلسطيني |
فرط ضغط الدم الرئوي
| فرط ضغط دموي رئوي | |
|---|---|
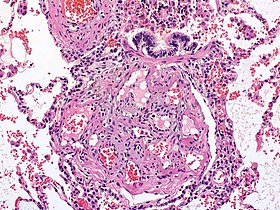
آفه ضفيرية - فرط ضغط الدم الرئوي
| |
| تعديل مصدري - تعديل |
فرط ضغط الدم الرئوي (بالإنجليزية: Pulmonary Hypertension) هو زيادة ضغط الدم داخل الشريان الرئوي أو الوريد الرئوي أو الشعيرات الدموية الرئوية (جميعها تعرف بالأوعية الرئوية أو أوعية الدورة الدموية الصغرى)، وزيادة الضغط في هذه الأوعية يؤدي إلى ظهور بعض الأعراض كضيق النّفس، الدوار، الإغماء، تورّم القدم والعديد من الأعراض الأخرى، التي تتفاقم جميعها مع ازدياد المجهود الجسدي. من الممكن أن يكون فرط ضغط الدّم الرئوي شديد جداً، مما يؤدي إلى قلة تحمل الجسم للتمارين الرياضيّة، تماماً كما يحدث في حالات الفشل القلبي. أول من تعرف على هذا المرض هو الدكتور إيرنست فون رومبيرج في عام 1891.[1] بناءً على أحدث التصنيفات، يمكن تقسيم فرط ضغط الدم الرئوي إلى ستة أنواع مختلفة (كما هي مذكورة في الأسفل).[2]
علامات وأعراض المرض

الأعراض بشكل عام تتطور تدريجيا وبشكل بطيء (أي تأخذ وقتا لتصبح واضحة للمريض) مما يؤخر زيارة المريض للطبيب عدة سنوات. أكثر الأعراض شيوعاَ هي:
- ضيق النفّس
- الاعياء
- السّعال الجّاف
- الذبحة الصدرية
- الإغماء أو فقدان الوعي
- ذمة الاطراف (الاستسقاء والتورّم حول الكاحل والقدم) ونادرا ما قد يحدث نفث الدم (سعال مصحوب بدم).
فرط ضغط الدم الرئوي الوريدي (الذي يكون في الوريد الرئوي) يَظهر عادةً مع أعراض ضيق النفس الإضّجاعي أو ضيق النَفس اللَّيلِي الانتيابي (وهو ضيق النفس عند الاضجاع أو النوم)، بينما فرط ضغط الدم الرئوي الشرياني لا يُظهر هذا النوع من الأعراض. يتم أخذ تاريخ عائلي شامل لتحديد ما إذا كان المرض متوارث عائلياَ. وأخذ تاريخ التّعرّض لبعض أنواع الأدوية والمواد مثل الكوكايين، الميثامفيتامين، الإيثانول (الذي يؤدي إلى التشّمع الرئوي) والتّبغ (الذي يؤدي إلى نُفاخ الرئة). يتم إجراء الفحص السريري للبحث عن علامات فرط ضغط الدم الرئوي، من هذه العلامات انفصال صوت القلب الثاني (S2) وارتفاع صوت انغلاق الصمام الرئوي بالإضافة إلى صوت رفيع (كصوت التنهيدة) يتم سماعه بجانب عظمة القص والذي يشير إلى تضّخّم في عضلة الأُذين الأيمن في القلب. قد يحدث احتقان عام في أجهزة الجسم المختلفة نتيجة فشل الجانب القلبي الأيمن، ومن علاماته تمدد الوريد الوداجي، الوذمة القدميّة (تجمع السوائل في القدم)، الاستسقاء، المنعكس الكبدي الوداجي، التعجّر وغيرها. يتم البحث أيضاً عن دلائل قصور الصمام ثلاثي الشرفات ودلائل قلس الصمام الرئوي (ارتجاع الصمام الرئوي) حيث يعتبر وجودها دليل على وجود فرط ضغط الدم الرئوي.
أسباب المرض وتصنيفاته
في عام 1973 تم عقد أول اجتماع يسعى لوضع تصنيفات لمرض فرط ضغط الدم الرئوي من قبل منظمة الصحة العالمية. تم فيه توضيح الفرق بين فرط ضغط الدم الرئوي الأوّلي وفرط ضغط الدم الرئوي الثانوي، ثم تم تقسيم فرط ضغط الدم الرئوي الأوّلي إلى «الآفات الشريانية» و «الوريدي الانسدادي» و «المتعلق بالامراض التخثرية والانصمامية».[3] تمّ عقد مؤتمر آخر عام 1998 في مدينة ايفيان الفرنسية بُيّنت فيه اسباب فرط ضغط الدم الرئوي الثانوي (الثانوي هو الناتج عن امراض أخرى أدّت إلى حدوثه).[4] وفي عام 2008، عُقدت رابع ندوة تتحدث عن فرط ضغط الدم الرئوي الشرياني في دانا بوينت في كاليفورنيا لتعديل التصنيفات بناء على المفهومات الجديدة التي توضّحت حول آلية حدوث المرض. النظام المعدّل الذي تم تطويره بواسطة هذه المجموعة هو الأساس الحالي في فهم مرض فرط ضغط الدم الرئوي.[2] النظام يحوي عدة تعديلات وتحسينات عمّا كان عليه نظام البندقية (فينيجيا) التصنيفي السابق عام 2004. يمكن تلخيص نظام دانا بوينت التصنيفي المُحَدّث لعام 2008 كالتّالي:[2]
المجموعة الأولى ضمن منظمة الصحة العالمية - فرط ضغط الدم الرئوي الشرياني:
- فرط ضغط الدم الرئوي الشرياني مجهول السبب.
- فرط ضغط الدم الرئوي الشرياني الوراثي.
أسبابه:
- طفرة في جين المستقبل المسؤول عن بروتينات تكوين العظم BMPR2.
- طفرة في جين ALK1 و endoglin المسؤولين عن إنتاج المُستقبل الخاص بعامل النمو (β-TGF)، قد يكون مصحوب بمرض توسع الشعيرات النزفي الوراثي والذي أساسه هو الطفرة في هذه الجينات.
- طفرة مجهولة.
- فرط ضغط الدم الشرياني الرئوي الناتج من الأدوية والسموم.
- فرط ضغط الدم الشرياني الرئوي المصحوب بــ
- مرض النَسيج الضام.
- الإصابة بفايروس الإيدز HIV
- فرط ضغط الدم البابي
- أمراض قلب خلقية
- البلهارسيا
- فقر الدم الانحلالي المزمن (مثل الانيميا المنجلية).
- فرط ضغط الدم الرئوي المستمر عند الأطفال حديثي الولادة.
- يتفرّع من هذه المجموعة فرع ثانوي يحوي مرض «الانسداد الوريدي الرئوي» ومرض «الوُرام الوعائي في الشعيرات الدموية الرئوية».
المجموعة الثانية ضمن منظمة الصحة العالمية - فرط ضغط الدم الرئوي الناتج عن أمراض الجانب الأيسر من القلب:
- خلل في الانقباض.
- خلل في الانبساط.
- امراض في صمامات القلب.
المجموعة الثالثة ضمن منظمة الصحة العالمية - فرط ضغط الدم الرئوي الناتج عن أمراض الرئة أو قلة الأوكسجين:
- الداء الرئوي المُسِد المزمن.
- داء الرئة الخلالي.
- أمراض رئوية أخرى تجمع بين الأمراض الانسدادية وأمراض التقييد.
- اضطراب النفس أثناء النوم.
- اضطرابات نقص التهوية في الحويصلات.
- التعرض المزمن للمرتفعات العالية.
- تشوهات رئوية خلقية أثناء النمو.
المجموعة الرابعة ضمن منظمة الصحة العالمية - فرط ضغط الدم الرئوي بسبب أمراض تخثرية أو انصمامية مزمنة:
- انصمام رئوي في الشرايين الرئوية القصوى والدنيا (القريبة والبعيدة).
- انصمامية بواسطة أشياء أخرى مثل خلايا ورمية.
المجموعة الخامسة في منظمة الصحة العالمية - فرط ضغط الدم الرئوي الناتج عن أسباب مختلفة ذات آليات غير واضحة:
- أمراض الدم: أمراض تكاثرية نقوية، إزالة الطحال.
- أمراض على مستوى أجهزة الجسم: داء الساركويد، داء منسجات خلايا لانجيرهانز الرئوي، ورم عضلي في الاوعية اللمفاوية والدّموية، ورم ليفي عصبي، التهاب الأوعية الدموية.
- أمراض الاضطرابات الأيضية: داء اختزان الجلايكوجين، داء غوشيه، داء الغدة الدرقية.
- أمراض أخرى: انسداد ورمي، التهاب المنصف الليفي، فشل كلوي المزمن.
طريقة توّلد المرض
أياً كان السبب الرئيسي للمرض، إنّ فرط ضغط الدم الرئوي الشرياني (الذي يصنف ضمن مجموعة منظمة الصحة العالمية الأولى) يحدث بسبب تضيق الأوعية الدموية الموجودة داخل الرئتين. مما يصّعب على القلب ضخ الدم إلى الرئتين، تماماً كما يحدث في حالة ضخ الماء خلال أنبوبة ضيقة مقارنةً مع ضخه خلال أنبوبة واسعة. مع مرور الزمن فإن الأوعية الدموية المتضررة تصبح أكثر صلابة وغلاظة بسبب عملية تسمى التليف، مما يسبب لاحقاً زيادة في ضغط الدم داخل الرئة وإعاقة لتدفق الدم خلالها. تشترك جميع أنواع فرط ضغط الدم الرئوي بأن زيادة الجهد المبذول على القلب يؤدي إلى تضخم في عضلة البطين الأيمن مما يجعل القلب أقل قدرة على ضخ الدم إلى الرئتين مسبباً ما يعرف بالفشل القلبي الأيمن (فشل الجانب الأيمن من القلب) وتسمى هذه الحالة كور بالمونيلا. البطين الأيمن يكون عادةَ تحت تأثير نظام يعتمد على الضغط المنخفض، حيث يكون الضغط فيه جزء من ستة أجزاء الضغط الموجود في البطين الأيسر. ولهذا فإن البطين الأيمن لا يستطيع التعامل مع ضغط بارتفاع ذاك الموجود في البطين الأيسر، حتى مع أن تضخم عضلات البطين قد تساعده في بادئ الأمر، لكن مع مرور الزمن وزيادة التضخم فإنه يصل إلى حالة لا تستطيع معها العضلات الحصول على الأوكسجين الكافي لعملها مما يؤدي إلى الفشل القلبي الأيمن. مع قلة تدفق الدم إلى الرئتين، يقل الدم المتدفق إلى البطين الايسر (لأن القلب أصبح يستقبل كمية أقل من الدم)، هذا الدم عادة يكون محمل بكمية أقل من الأوكسجين. مما يقلل من كمية الدم المنتقلة إلى باقي الجسم عبر الدورة الدموية الكبرى خاصةَ أثناء زيادة النشاطات البدنية.
طريقة تولد فرط ضغط الدم الرئوي الناتج عن فشل الجانب الأيسر من القلب (الموجود ضمن مجموعة منظمة الصحة العالمية الثانية) تختلف تماما عن الطريقة السابقة لأنها لا تشمل أي تضيق أو تلف في الأوعية الدموية الرئوية. لكن بدلاً عن ذلك، فإن الجانب الأيسر للقلب يفشل في ضخ كمية كافية من الدم مما يؤدي إلى تجمع الدم داخل الرئتين وتولد ضغط ارتجاعي داخل الدورة الدموية الصغرى. هذا يؤدي إلى أمراض مثل وذمة الرئة (استسقاء الرئة) وانصبابات جنبيّة (تجمع سوائل رئوية).
في فرط ضغط الدم الرئوي الناتج عن نقص الأوكسجين (المجموعة الثالثة ضمن منظمة الصحة العالمية) فإن قلة مستوى الأوكسجين يؤدي إلى تضيق الشرايين الرئوية، هذه الظاهرة تسمى «تضيق الاوعية الدموية الرئوية الناتجة عن نقص الأوكسجين»، هذه الظاهرة تحدث لحماية ومنع الدم من التدفق إلى الأماكن المتضررة بالرئة والتي لا تحوي أوكسجين، لكن إذا كان الضرر في الرئة كبير وُمطوّل، فإن ظاهرة تضيق الاوعية الدموية بفعل نقص الأوكسجين تصبح واسعة لتشمل نسبة كبيرة من الأوعية الرئوية.
في فرط ضغط الدم الرئوي الناتج عن الأمراض التخثرية أو الانصمامية المزمنة (المجموعة الرابعة في منظمة الصحة العالمية)، فإن الأوعية الدموية تغلق أو تتضيق بفعل جلطات دموية متكررة، هذه الجلطات قد تفرز مواد تؤدي إلى تضيق في الأوعية الدموية. هذا التعاون بين انسداد الأوعية الدموية بفعل الجلطة وتضيّقها بفعل المواد المفرَزة يزيد من مقاومة الأوعية لتدفق الدم مما يؤدي إلى زيادة ضغط الدم داخل الدورة الدموية الصغرى.
علم الأمراض الجزيئي الخاص بالمرض
آلية الإصابة بفرط ضغط الدم الرئوي على مستوى الجزيئات غير معروفة بعد، لكن من المتوقع أن اختلال الاغشية البطانية يؤدي إلى قلة إنتاج المواد المضيقة للأوعية الناتجة عن الأغشية البطانية مثل أكسيد النتريك والبروستاسايكلين. بالإضافة إلى وجود تحفيز لإنتاج مواد مضيقة للأوعية الدموية مثل الثرومبوكسان وعامل النمو الوعائي البطاني. كل هذا يؤدي إلى خواص تضيق الاوعية الدموية وتضخم العضلات الملساء التي يتميز بها مريض فرط ضغط الدم الرئوي الشرياني.[5]

في الوضع الطبيعي، إنزيم صانع أكسيد النتريك يُنتج أكسيد النتريك من ل-أرجينين في وجود الأوكسجين. يتم تفعيل إنزيما مُحلّق الادنيلات (يكّون منها حلقات) ومّحلّق الجوالينات في وجود أكسيد النتريك، هذان الإنزيمان ينتجان أحادي فسفات الأدنوسين الحلقي وأحادي فسفات الجوانوسين الحلقي على التوالي. يتم إنتاج أحادي فسفات الجوانوسين الحلقي بواسطة نوع من الإنزيمات محلّقة الجوالينات (الذي هو نوع من أنواع الإنزيمات المُحلّقة لانزيم البايروفسفات): إنزيم مُحلّق الجوانيلات القابل للذوبان، الذي يقوم بتسريع عملية إنتاج أحادي فوسفات الجوانوسين الحلقي من ثلاثي فوسفات الجوانوسين. إنزيم مُحلّق الجوانيلات هو مركب مكوّن من وحدتين مختلفتين، وحدة ألفا ووحدة بيتا في كل سلسلة. وهو يحوي أيضا مجموعة هيم اللازمة لارتباط أكسيد النتريك. الاتحاد بين إنزيم مُحلّق الجوانيلات وأكسيد النتريك يُنتج تغييرات تركيبية في تكوين الإنزيم التي تؤدي إلى تحفيز إنتاج احادي فوسفات الجوانوسين الحلقي.[6]
في الأغشية البطانية للأوعية، يقوم أحادي فوسفات الجوانوسين الحلقي بتفعيل إنزيم كيناز أحادي فسفات الجوانوسين الحلقي (بروتين كيناز ج)، هذا الإنزيم يعود إلى كيناز نوع محدد من بروتين سيرين/ثريونين. بروتين كايناز ج هو دايمر (مركب جزيئي مكون من مركبين متشابهين) مكون من سلسلتي عديد ببتيد متشابهتين يتشاركان نفس التركيب الجزيئي. كل وِحدة منهما تتكون من قِطاع محفّز وقِطاع منظّم. يقوم إنزيم كايناز أحادي فوسفات الجوانوسين بتفعيل قنوات البوتاسيوم وتثبيط قنوات الكالسيوم، هذه العملية تؤدي إلى تقليل نسبة الكالسيوم داخل الخلايا وحدوث توسّع في الأوعية الدموية.[7] إنزيم فوسفودايسترايز النوع الخامس، والموجود بكثرة في الأنسجة الرئوية، هو إنزيم محلل للروابط الفلزية باستخدام جزيئات الماء، يقوم بتحليل الرابطة الحلقية في أحادي فوسفات الجوانوسين الحلقي في وجود أيون الزنك. في الحقيقة، اتحاد أيون الزنك مهم جدا لعمل إنزيم فوسفودايسترايز الخامس. هناك سلسة حمض أميني عند الطرف الأميني (القطاع المنظم) لإنزيم فوسفودايسترايز الخامس تقوم بربط أحادي فسفات الجوانوسين الحلقي. هذه السلسة مقسمة إلى قِطاعين؛ جاف-أ وجاف-ب؛ لكن فقط جاف-أ هي التي تملك الألفة (الانجذابية) الكافية للارتباط مع أحادي فسفات الجوانوسين الحلقي. هذا الاتحاد يزيد من نشاط الإنزيم في التحفيز وهو مثبّت بواسطة الحمض الأميني سيرين (المضاف بواسطة عملية فسفرة بإنزيم كايناز). وبناءً على هذا، فإن تركيز أحادي فسفات الجوانوسين الحلقي ينخفض مما يؤدي إلى توقف التوسعة في الأوعية.[7]
يقوم الأشخاص المصابين بمرض فرط ضغط الدم الرئوي الشرياني بإنتاج كميات أقل من أكسيد النتريك والمواد الأخرى الموسعة للأوعية الدموية وإنتاج كميات أكبر من المواد المضيّقة للأوعية. وبناءً على هذا، يكون المسار الجزيئي غير منتظم مؤدياً إلى تضيّق ثابت في الأوعية الدموية. لهذا فإن أكسيد النتيرك ومثبطّات إنزيم فوسفودايسترايز الخامس مثل تادالافيل وسلدينافيل هي إحدى الأدوية المستخدمة لعلاج هذا المرض.[7] فعلى سبيل المثال، تادالافيل يقوم بعمل توسعة للأوعية الدموية بمساعدة أكسيد النتريك الموجود في البطانة الداخلية للأوعية الرئوية.
تشخيص المرض

لان فرط ضغط الدم الرئوي يتكون من خمس أنواع رئيسية -فرط ضغط الدم الرئوي الشرياني، الوريدي، الناتج عن قلة الاوكسجين، الناتج عن الامراض التخثرية والانصمامية والناتج عن آليات متنوعة- ؛ فانه يتم إجراء سلسلة من الاختبارات للتفريق بينها. يتم عمل اجراءات لاحقة للتأكد من وجود فرط ضغط الدم الرئوي واستثناء الامراض الأخرى، هذه الاجراءات تشمل: اختبار وظائف الرئة؛ تحليل الدم لاستبعاد امراض الايدز والكبد وأمراض المناعة الذاتية؛ مخطط كهربائية القلب؛ قياسات غازات الدم الشرياني؛ صورة أشعة سينية للصدر (متبوعة بصورة طبيقية عالية الوضوح إذا تم الشك بوجود امراض رئوية خِلاليّة)؛ واختبار التهوية/التدفق لاستبعاد فرط ضغط الدم نتيجة الامراض التخثرية والانصمامية المزمنة. لا يتم أخذ خزعة من الرئة الا إذا تم الشك بحدوث فرط ضغط الدم نتيجة لامراض رئوية خلالية؛ أيضاً، هناك تخوّفات ان خزعات الرئة قد تسبب نزيف نتيجة الضغط الرئوي البيني العالي. يتم أيضا قياس درجة التحسن طبيّاً عن طريق «اختبار السير لمدة 6 دقائق», بمعنى آخر، يتم حساب المسافة التي يستطيع ان يقطعها المريض خلال 6 دقائق. كلّما كانت نتائج هذا القياس ثابتة ومتحسنة فهي دليل على وجود فرص أفضل للنجاة.

من المطلوب وجود فرط في ضغط الدم الرئوي لتشخيص مرض فرط ضغط الدم الرئوي الشرياني. على الرغم من ان ضغط الشريان الرئوي يمكن تقديره بواسطة مخطط صدى القلب، لكن قياسات الضغط بواسطة قسطرة سوان-جانز من خلال الجانب الأيمن للقلب توفر الوسيلة الأفضل للقياس. ضغط الشريان الرئوي الانسدادي ومقاومة الاوعية الرئوية لا يمكن حسابها مباشرة من مخطط صدى القلب. لهذا فان تشخيص فرط ضغط الدم الرئوي الشرياني يتطلب قسطرة من الجانب الأيمن للقلب. قسطرة سوان-جانز تستطيع أيضا قياس مخرجات القلب، والتي تعتبر أكثر أهمية في حساب حِدّة المرض من قياس ضغط الشريان الرئوي. متوسط الضغط الشرياني الرئوي الطبيعي لشخص يعيش على مستوى سطح البحر يساوي تقريبا 8-20 مم زئبقي في حالة الراحة. فرط ضغط الدم الرئوي يحدث عندما يتجاوز الضغط الشرياني الرئوي 25 مم زئبقي في حالة الراحة.[8] لا يجب الخلط بين «متوسط الضغط الشرياني الرئوي» وبين «الضغط الشرياني الرئوي الانقباضي», والذي يُسجل غالباً في بيانات مخطط صدى القلب. إذا كان الضغط الشرياني الرئوي الانقباضي يساوي 40 مم زئبقي فان متوسط الضغط الشرياني الرئوي يساوي 25 مم زئبقي. حِسابياً، فان متوسط الضغط الشرياني الرئوي =0.61 * الضغط الشرياني الرئوي الانقباضي + 2.
الفحص السريري
يتم القيام بالفحص السريري للبحث عن الاعراض الاعتيادية لفرط ضغط الدم، وهي تشمل تغيّر في اصوات القلب، مثل انفصال واسع في الصوت الثاني للقلب، ارتفاع صوت انغلاق الصمام الرئوي (هو جزء من صوت القلب الثاني), صوت كالنهدة يتم سماعه بجوار عظمة القص، وجود وسماع الصوت الثالث للقلب (الذي يكون عادةً غير مسموع) وارتجاع رئوي. هناك علامات أخرى تشمل ارتفاع الضغط في الوريد الوداجي، وذمة طرفيّة (استسقاء في الاطراف كالكاحل والقدم), استسقاء في البطن نتيجة تجمع السوائل، انعكاس كبدي وداجي وتعجّر الأصابع والأظافر (تخن النهايات).
مخطط صدى القلب
يتم عمل تحليل ميتا عن طريق صدى الصوت الناتج عن تأثير دوبلر للتنبؤ بالقسطرة، هذا يعطي حساسية بنسبة 88% وفعالية بنسبة 56%.[9]
العلاج
يتم تحديد طريقة العلاج بناءً على إذا ما كان فرط ضغط الدم الرئوي هو شرياني أو وريدي أو ناتج عن نقص الأوكسجين أو انصمامي تخثري أو ناتج عن عوامل أخرى. بما أن فرط ضغط الدم الرئوي الوريدي يأتي مترادفاً مع فشل القلب، يكون العلاج أساساً لتحسين وظيفة البطين الأيسر باستخدام مدرّات البول، مضّادات بيتا، مثبطّات الانزيم المحوّل للانجوتنسين، وغيرها، أو عن طريق إصلاح/استبدال الصمام ثنائي الشرفات (التاجي) أو الصمام الأورطي. لا ينبغي معالجة المرضى الذين يعانون من فشل الجانب الأيسر للقلب أو أمراض الرئة الناتجة عن نقص الأكسجين (المجموعتين الثانية أو الثالثة لفرط ضغط الدم الرئوي) بالعلاج الروتيني باستخدام المواد الفعّالة في الأوعية الدموية مثل البروستانويدات أو مثبطّات انزيم فوسفودايستريز أو مضادات مستقبل الاندوثيلين، والتي تستخدم لعلاج حالة فرط ضغط الدم الرئوي الشرياني. من أجل التمييز بين أنواع فرط ضغط الدم يقوم الأطباء بعمل قسطرة للجانب الأيمن من القلب، مخطط صدى القلب، تصوير مقطعي للصّدر، اختبار المشي لمدة ست دقائق واختبار وظائف الرئة.[10] استخدام مرضى هذه الحالات لأدوية أخرى مخصصة لعلاج أنواع أخرى من فرط ضغط الدم الرئوي قد يسبب ضرراً للمريض واستنزاف للموارد الطبية الضرورية.[10] الجرعات الكبيرة من مثبطّات قنوات الكالسيوم مفيدة فقط لـ 5% من مرضى فرط ضغط الدم الرئوي الشرياني مجهول السبب والخاضعين لقسطرة سوان-جانز. لقياس تأثير الأدوية على أوعيتهم الرئوية. لسوء الحظ، انتشر الاستخدام الخاطئ لمضادات قنوات الكالسيوم بشكل كبير، لأن إعطاءها لمرضى فرط ضغط الدم الرئوي الشرياني الغير خاضعين للقسطرة، تؤدي إلى زيادة نسب الإصابة والوفيّات. تم تغيير معايير قياس تأثير الأدوية على الأوعية الرئوية. المرضى الذين ينخفض لديهم متوسط ضغط الدم الرئوي الشرياني بمقدار 10-40 مم زئبقي (مع عدم تغيّر أو زيادة مخرجات القلب عند إعطاءهم أدينوسن، إبوبروستينول أو أكسيد النتريك) هم فقط القابلين لقياس تأثير الأدوية على أوعيتهم الرئوية.[11] يستجيب نصف هؤلاء المرضى فقط لمضادات قنوات الكالسيوم على المدى الطويل.[12] هناك بعض الأدوية تم استحداثها لفرط ضغط الدم الرئوي الشرياني الأوّلي والثانوي. التجارب التي قامت بدعم استخدام هذه المواد هي قليلة نسبياً، القياس الوحيد المستخدم لمقارنة فعاليتها هو «اختبار السّير لمدة 6 دقائق». لا يوجد للعديد منها أي معلومات عن فوائدها في تقليل نسب الوفيّات.[10]
موّاد فعّالة في الأوعية الدموية
هناك عدّة مسارات (آليّات) مسؤولة عن الانقباض والتكاثر غير الطبيعي لخلايا العضلات الملساء داخل الشرايين الرئوية لمرضى فرط ضغط الدم الرئوي الشرياني. ثلاثة من هذه المسارات هي غاية في الأهمية لأنها مُستهدفة من قبل هذه الأدوية – مضادات مستقبل الاندوثيلين، مثبطّات النوع الخامس من إنزيم فوسفودايستريز ومشتقّات البروستاسايكلن. لان الأدوية قليلة التكلفة غير متوفرة بشكل كبير، لم تقم منظمة الصحة العالمية في إدراجهم ضمن قائمة الأدوية الأساسية لفرط ضغط الدم الرئوي.
بروستاجلاندين
بروستاسايكلن (بروستاجلاندين آي2) يعتبر أكثر الأدوية شيوعاً وكفاءة في علاج فرط ضغط الدم الرئوي الشرياني. إيبوبروستينول (هو بروستاسايكلن صناعي يسوّق تحت مسمى فلولان) يُعطى عن طريق محلول ثابت يتطلّب قسطرة وريدية مركزية شبه دائمة. نظام إعطاء هذا الدواء قد يسبب تلوث للدم بالمايكروبات وتكوّن جلطات. تركيب البروستاسايكلن غير مستقر، لهذا يجب إبقاؤه داخل الثلج طوال فترة إعطاؤه للمريض. بما أن نصف العمر له يساوي 3-5 دقائق، فيجب إعطاؤه بانتظام طوال الوقت (24/7)، وأي انقطاع في إعطاؤه قد يكون قاتل. لهذا تم تطوير أدوية أخرى من البروستانويدات. تريبروستاينيل (ريموديولين) يمكن إعطاؤه داخل الوريد أو تحت الجلد. لكن إعطاؤه تحت الجلد قد يكون مؤلم للغاية، أعلن مركز مكافحة الأمراض أن إعطاء الريموديولين عن طريق الوريد قد يزيد من فُرص تلوّث الدم بالمايكروبات. إيلوبروست (يُسوّق تحت اسم فينتافيس) كان الدواء الوحيد من نوع بروستاسايكلن الذي يؤخذ عن طريق الاستنشاق والذي تم الموافقة على استخدامه من قبل أمريكا وأوروبا، إلى أن تم الموافقة عام 2009 على نوع دواء مستنشق من تريبروستاينيل مُسوّق تحت اسم تيفاسو. النوع المستنشق من الأدوية له حسنات أكثر لأنه يستهدف الرئة مباشرة مسببا أعراض جانبية أقل، مع ذلك فإنه عادةً ما يكون هناك سعال والتهاب للحلق. أنواع دواء ريموديولين التي يمكن أخذها عن طريق الفم أو الاستنشاق لا تزال قيد التطوير. بيرابروست هو نوع بروستانويد يعطى عن طريق الفم متوّفر في كوريا الجنوبية واليابان.
مضادات مستقبل الاندوثيلين
بوسينتان (معروف تجارياً بـ تراكلير) هو مضّاد مستقبل اندوثيلين ازدواجي الوظيفة (يعمل على مستقبل اندوثيلين نوع أ ونوع ب) تمّ اعتماده في عام 2001. سيتازنتان (ثيلين)، هو مضاد مستقبل اندوثيلين اختياري الوظيفة، يعمل فقط على مستقبل اندوثيلين نوع أ، تمّ اعتماد استخدامه في كندا، أستراليا والاتحاد الأوروبي.[13] لكن لم يتم اعتماده في الولايات المتحدة الأمريكية. في عام 2010، قامت شركة فايزر بسحب الثيلين من الأسواق بسبب مضاعفاته القاتلة على الكبد. أمبريسنتان، هو دواء مشابه للثيلين تم بيعه في الولايات المتحدة الأمريكية من قبل شركة غيلياد ساينسز تحت اسم ليتايرز.[14] بالإضافة إلى ذلك، يتم منذ عام 2008 اخضاع مضّاد مستقبل اندوثيلين ازدواجي الوظيفة جديد للتجارب السريرية؛ أستليون-1، والذي تم إنتاجه من نفس الشركة المُصنعة لتراكلير.
مثبطّات النوع الخامس من انزيم فوسفودايستريز
قامت المؤسسة العامة للغذاء والدواء في الولايات المتحدة الأمريكية عام 2005 بالموافقة على دواء سايلدينافيل؛ وهو مثبّط لإنزيم فوسفودايستريز الخامس الخاص بأحادي فسفات الجوانوسين الحلقي؛ كعلاج لفرط ضغط الدم الرئوي الشرياني. يتم بيعه في الأسواق تحت اسم ريفاشو. أيضا تم الموافقة على تادالافيل عام 2009 وهو نوع آخر من مثبطّات إنزيم فوسفودايستريز الخامس، ويتم تسويقه تحت المسمى آدسيركا.[15] تقوم أدوية مثبطّات فوسفودايستريز بتوسعّة الاوعية الدموية، وتثبيط إعادة تشكيل الأوعية الدموية، مؤدية إلى تقليل الضغط الرئوي الشرياني وتقليل المقاومة في الأوعية الرئوية. يتم أخذ تادالافيل وسايلدانافيل عن طريق الفم، ويتم امتصاصهما داخل القناة الهضمية بفاعليّة كبيرة (تظهر مستوياتهم في الدم بعد 20 دقيقة من أخذ الدواء). الجرعة المُوصى بها هي 40 مل جرام مرّة واحدة في اليوم، وعمر النصف يكون 17.5 ساعة في الأشخاص السليمين.[16] أيضاً، إذا تم أخذ العامل المّادي في عين الاعتبار، فإن المريض الذي يتناول تادالافيل قد يدفع 33% أقل من سعر دواء السايلدينافيل.[17] هناك بعض الأعراض الجانبية للدواء كالصدّاع، الإسهال، الغثيان، آلام الظهر، سوء الهضم، احمرار الوجنتين وألم العضلات.[18]
منشطّات انزيم جوانيلات سايكليز القابل للذوبان
إنزيم جوانيلات سايكليز القابل للذوبان هو عبارة عن مستقبل داخل خلوي لأكسيد النتريك. في أبريل عام 2009، تم اخضاع منشطّات إنزيم جوانيلات سايكليز القابل للذوبان؛ سيناسيجوات وريوسيجوات؛ تحت التجربة لمعرفة إمكانيتها على علاج فرط ضغط الدم الشرياني الرئوي. وفي أكتوبر عام 2013، تمت الموافقة على ريوسيجوات (أديمباز) من قبل المؤسسة العامة للغذاء والدواء كعلاج لفرط ضغط الدم الرئوي الشرياني، وكان الأول من نوعه.
العلاج جراحياً

تَقب الحاجز الأذيني، هو إجراء جراحي يتم فيه عمل فتحة للوصل بين الأذين الأيمن والأيسر. وهو يقوم بتخفيف الضغط على الجانب الأيمن من القلب، لكن هذا يكون على حساب خفض مستويات الأوكسجين في الدم. تقوم عملية زراعة الرئة بعلاج فرط ضغط الدم الرئوي الشرياني، لكنها تترك المريض عُرضة لمضاعفات العملية ومتوسط نسبة نجاة خمس سنوات بعد العملية.[19] عملية استئصال الخثرة الرئوية وبطانة الشريان، هي عملية جراحية تستخدم لعلاج فرط ضغط الدم الرئوي الناتج عن أمراض تخثرية وانصمامية مزمنة. يتم فيها إزالة الخثرة المنتظمة حول البطانة الداخلية للشريان؛ وهي عملية صعبة جداً، لا يتم إجراءها إلا في القلة القليلة من المراكز المُختارة فقط. لا يوجد إجراء علاجي محدد لفرط ضغط الدم الرئوي الناتج عن قلّة الأوكسجين أو الأنواع المختلفة الأخرى. ومع ذلك، يوجد دراسات تجرى حالياً على المرضى لاختبار بعض العوامل العلاجية. يقوم أغلب الأطباء في الوقت الراهن بعلاج هذه الحالات باستخدام نفس الأدوية المستخدمة لعلاج فرط ضغط الدم الرئوي الشرياني، إلى أن تتوفر لها خيارات أفضل للعلاج. يسمى هذا النوع من العلاج بالعلاج خارج التخصيص (وهو استخدام أحد الأدوية لعلاج مرض غير ذلك الذي خُصص لعلاجه).
المُراقبة
إرشادات التدريب السريري المقررة تحدّد مقدار تكرار عملية التقييم والمراقبة للعقد الرئوية،[20] يتم مراقبة المرضى عادة باختبارات شائعة ومتوفرة مثل:
- قياس تأكسج النبض (قياس التأكسج: هو قياس كمية الأوكسجين في المادة).
- قياس غازات الدم الشرياني.
- صورة أشعة سينية للصدر.
- مخطط كهربائية القلب.
- مخطط صدى القلب.
- قياس وظائف الرئة (سبايرومتري).
توقعات سير المرض
أظهرت سجلات معاهد الصحة الوطنية الأمريكية لفرط ضغط الدم الرئوي عام 1980 أن متوسط النجاة للمرضى غير الخاضعين للعلاج هو 2-3 سنوات من وقت التشخيص بالمرض. وعادةَ ما يكون سبب الوفاة هو فشل وقصور في البطين الأيمن. ثم أظهرت نتائج دراسة حديثة قامت بتجربة العلاج بواسطة دواء بوسينتان أن 89% من المرضى كانو أحياء بعد سنتين.[21] تغيرت نتائج المرض بشكل جذري للأفضل منذ العقدين الأخيرين، وذلك بسبب العلاجات الجديدة بالأدوية والعناية الصحية الجيدة والتشخيص المبكر. على سبيل المثال، ارتفع متوسط البقاء لـ 2635 من المرضى المسجلين في - سجلّات تحسين العناية بفرط ضغط الدم الرئوي الشرياني المبكر وطويل الأمد- في الفترة من مارس 2006 إلى ديسمبر 2009, كانت معدلات البقاء لمدة سنة، 3 سنوات، 5 سنوات، 7 سنوات هي 85٪، 68٪، 57٪، و 49٪ على التوالي. أما بالنسبة للمرضى الذين كانوا يعانون من ارتفاع ضغط الدم الرئوي مجهول السبب أو الوراثي كانت معدلات البقاء لهم هي 91٪، 74٪، 65٪، و 59٪ على التوالي.[22] تكون معدلات الوفيات عالية جداً في النساء الحوامل المصابات بفرط ضغط الدم الرئوي الحاد. وأحينا ما يتم منع النساء المصابات بهذا المرض من الحمل حفاظا على حياتهن.[23][24][25]
في علم الوبائيّات
يعتبر فرط ضغط الدم الرئوي الشرياني مجهول السبب نادراً. حيث إنه يصيب 2-3 أشخاص سنوياً. بمعدل انتشار 15 لكل مليون تقريباً. الإناث البالغات يكّن 3 مرات أكثر عرضةً من الذكور البالغين. بينما معدّلات الإصابة به عند الأطفال موّزعة بالتساوي بين الذكور والإناث. أنواع فرط ضغط الدم الرئوي الشرياني الأخرى تعد أكثر انتشارا وشيوعاً. في المرضى المصابين بتصلب الجلد تكون معدلات الإصابة 6-60% من بين جميع المرضى، في مرضى التهاب المفاصل الروماتيدي تكون معدلات الإصابة 21%، في مرضى الذئبة الحُمامية معدلات الإصابة 4-14%، في فرط ضغط الدم البابي تكون بين 2 إلى 5%، في مرضى الإيدز تقريباً 0.5%، وفي مرضى الأنيميا المنجلية تتراوح معدلات الإصابة بين 20 إلى 40%. أقراص الحمية مثل فين-فين تسبب معدلات إصابة سنوية بمقدار 25-50 لكل مليون شخص.
معرض صور
مراجع
- ^ von Romberg, Ernst (1891–1892). "Über Sklerose der Lungenarterie". Dtsch Arch Klin Med (بالألمانية). 48: 197–206.
- ^ أ ب ت Simonneau G، Robbins I، Beghetti M، وآخرون (30 يونيو 2009). "Updated Clinical classification of pulmonary hypertension". J. Am. Coll. Cardiol. ج. 54 ع. 1 Suppl S: S43–S54. DOI:10.1016/j.jacc.2009.04.012. PMID:19555858. مؤرشف من الأصل في 2015-09-24.
- ^ Hatano S، Strasser R (1975). Primary pulmonary hypertension. Geneva: World Health Organization.
- ^ Rich S، Rubin LJ، Abenhail L، وآخرون (1998). Executive summary from the World Symposium on Primary Pulmonary Hypertension (Evian, France, September 6–10, 1998). Geneva: The World Health Organization. مؤرشف من الأصل في 2002-04-08.
- ^ Budhiraja R, Tuder RM, Hassoun. PM. Endothelial dysfunction in pulmonary hypertension. Circulation. 2004;109:159–165.
- ^ Fosfodiesterasas del AMPc y del GMPc en el cerebro: Expresión en procesos neuroinflamatorios y neurodegenerativos. URL: http://www.tesisenred.net/bitstream/handle/10803/891/03.ERI_METODOS.pdf?sequence=4. Viewed 3 November 2012.|Text in Spanish نسخة محفوظة 24 مارس 2021 على موقع واي باك مشين.
- ^ أ ب ت Ghofrani HA, Pepke-Zaba J, Barbera JA, et al. Nitric oxide pathway and phosphodiesterase inhibitors in pulmonary arterial hypertension. J Am Coll Cardiol. 2004;43:68S–72S.
- ^ Badesch، DB؛ Champion, HC; Sanchez, MA; Hoeper, MM; Loyd, JE; Manes, A; McGoon, M; Naeije, R; Olschewski, H; Oudiz, RJ; Torbicki, A (30 يونيو 2009). "Diagnosis and assessment of pulmonary arterial hypertension". Journal of the American College of Cardiology. ج. 54 ع. 1 Suppl: S55-66. DOI:10.1016/j.jacc.2009.04.011. PMID:19555859. مؤرشف من الأصل في 2016-06-24.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Taleb M، Khuder S، Tinkel J، Khouri SJ (2013). "The diagnostic accuracy of Doppler echocardiography in assessment of pulmonary artery systolic pressure: a meta-analysis". Echocardiography. ج. 30 ع. 3: 258–65. DOI:10.1111/echo.12061. PMID:23227919.
- ^ أ ب ت Torres F (2007). "Systematic review of randomised, double-blind clinical trials of oral agents conducted in patients with pulmonary arterial hypertension". Int. J. Clin. Pract. ج. 61 ع. 10: 1756–65. DOI:10.1111/j.1742-1241.2007.01545.x. PMID:17877662. مؤرشف من الأصل في 2007-12-22. اطلع عليه بتاريخ 2016-06-18.
- ^ Barst RJ، McGoon M، Torbicki A، وآخرون (يونيو 2004). "Diagnosis and differential assessment of pulmonary arterial hypertension". J. Am. Coll. Cardiol. ج. 43 ع. 12 Suppl S: 40S–47S. DOI:10.1016/j.jacc.2004.02.032. PMID:15194177.
- ^ Sitbon O، Humbert M، Jaïs X، وآخرون (يونيو 2005). "Long-term response to calcium channel blockers in idiopathic pulmonary arterial hypertension". Circulation. ج. 111 ع. 23: 3105–11. DOI:10.1161/CIRCULATIONAHA.104.488486. PMID:15939821. مؤرشف من الأصل في 2008-10-11.
- ^ "UPDATE 1-Encysive gets Canadian approval for hypertension drug". Reuters. 30 مايو 2008. مؤرشف من الأصل في 2009-01-09. اطلع عليه بتاريخ 2007-07-08.
- ^ "U.S. Food and Drug Administration Approves Gilead's Letairis Treatment of Pulmonary Arterial Hypertension" (Press release). غيلياد ساينسز. 15 يونيو 2007. مؤرشف من الأصل في 2013-03-06. اطلع عليه بتاريخ 2007-06-16.
- ^ "FDA approves Adcirca (tadalafil) tablets for pulmonary arterial hypertension" (Press release). 26 مايو 2009. مؤرشف من الأصل في 2014-07-04. اطلع عليه بتاريخ 2010-12-06.
- ^ Forgue ST, Patterson BE, Bedding. AW, et al. Tadalafil pharmacokinetics in healthy subjects. Br J Clin Pharmacol. 2005;61:280–288.
- ^ Sally A. Arif, PharmD, BCPS (Department of Pharmacy Practice, Chicago College of Pharmacy, Midwestern University, Downers Grove, Illinois, and Department of Pharmacy, Rush University Medical Center, Chicago, Illinois); and Henry Poon, PharmD, BCPS (Department of Pharmacy, James J. Peters VA Medical Center, Bronx, New York). Tadalafil: A Long-Acting Phosphodiesterase-5 Inhibitor for the Treatment of Pulmonary Arterial Hypertension. 2011;33:993–1004
- ^ Galié N, Brundage BH, Ghofrani HA, et al. Tadalafil therapy for pulmonary arterial hypertension. Circulation. 2009;119:2894–2903.
- ^ "2006 OPTN/SRTR Annual Report". US Scientific Registry of Transplant Recipients. 1 مايو 2006. مؤرشف من الأصل في 2014-12-22. اطلع عليه بتاريخ 2007-03-28.
- ^ American College of Chest Physicians؛ American Thoracic Society (سبتمبر 2013)، "Five Things Physicians and Patients Should Question"، اختر بحكمة: an initiative of the اختر بحكمة، American College of Chest Physicians and American Thoracic Society، مؤرشف من الأصل في 2020-03-13، اطلع عليه بتاريخ 2013-01-06, which cites
- McLaughlin، V. V.؛ Archer، S. L.؛ Badesch، D. B.؛ Barst، R. J.؛ Farber، H. W.؛ Lindner، J. R.؛ Mathier، M. A.؛ McGoon، M. D.؛ Park، M. H.؛ Rosenson، R. S.؛ Rubin، L. J.؛ Tapson، V. F.؛ Varga، J.؛ Harrington، R. A.؛ Anderson، J. L.؛ Bates، E. R.؛ Bridges، C. R.؛ Eisenberg، M. J.؛ Ferrari، V. A.؛ Grines، C. L.؛ Hlatky، M. A.؛ Jacobs، A. K.؛ Kaul، S.؛ Lichtenberg، R. C.؛ Lindner، J. R.؛ Moliterno، D. J.؛ Mukherjee، D.؛ Pohost، G. M.؛ Rosenson، R. S.؛ Schofield، R. S. (2009). "ACCF/AHA 2009 Expert Consensus Document on Pulmonary Hypertension: A Report of the American College of Cardiology Foundation Task Force on Expert Consensus Documents and the American Heart Association: Developed in Collaboration with the American College of Chest Physicians, American Thoracic Society, Inc., and the Pulmonary Hypertension Association". Circulation. ج. 119 ع. 16: 2250–2294. DOI:10.1161/CIRCULATIONAHA.109.192230. PMID:19332472.*Galie، N.؛ Hoeper، M. M.؛ Humbert، M.؛ Torbicki، A.؛ Vachiery، J. -L.؛ Barbera، J. A.؛ Beghetti، M.؛ Corris، P.؛ Gaine، S.؛ Gibbs، J. S.؛ Gomez-Sanchez، M. A.؛ Jondeau، G.؛ Klepetko، W.؛ Opitz، C.؛ Peacock، A.؛ Rubin، L.؛ Zellweger، M.؛ Simonneau، G.؛ Vahanian، A.؛ Auricchio، A.؛ Bax، J.؛ Ceconi، C.؛ Dean، V.؛ Filippatos، G.؛ Funck-Brentano، C.؛ Hobbs، R.؛ Kearney، P.؛ McDonagh، T.؛ McGregor، K.؛ Popescu، B. A.؛ وآخرون (2009). "Guidelines for the diagnosis and treatment of pulmonary hypertension: The Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS), endorsed by the International Society of Heart and Lung Transplantation (ISHLT)". European Heart Journal. ج. 30 ع. 20: 2493–2537. DOI:10.1093/eurheartj/ehp297. PMID:19713419.*Hoeper، M. M.؛ Barberà، J. A.؛ Channick، R. N.؛ Hassoun، P. M.؛ Lang، I. M.؛ Manes، A.؛ Martinez، F. J.؛ Naeije، R.؛ Olschewski، H.؛ Pepke-Zaba، J.؛ Redfield، M. M.؛ Robbins، I. M.؛ Souza، R. R.؛ Torbicki، A.؛ McGoon، M. (2009). "Diagnosis, Assessment, and Treatment of Non-Pulmonary Arterial Hypertension Pulmonary Hypertension". Journal of the American College of Cardiology. ج. 54 ع. 1 Suppl: S85–S96. DOI:10.1016/j.jacc.2009.04.008. PMID:19555862.
- ^ McLaughlin VV، Sitbon O، Badesch DB، وآخرون (2005). "Survival with first-line bosentan in patients with primary pulmonary hypertension". Eur. Respir. J. ج. 25 ع. 2: 244–9. DOI:10.1183/09031936.05.00054804. PMID:15684287. مؤرشف من الأصل في 2008-07-06.
- ^ Benza RL؛ Miller DP؛ Barst RJ؛ Badesch DB؛ Frost AE؛ McGoon MD. (أغسطس 2012). "An evaluation of long-term survival from time of diagnosis in pulmonary arterial hypertension from the REVEAL Registry". Chest. ج. 142 ع. 2: 448–56. DOI:10.1378/chest.11-1460. PMID:22281797. مؤرشف من الأصل في 2017-07-06. [FREE]
- ^ Kaufman, Matthew H.؛ Latha Stead؛ Feig, Robert (2007). First aid for the obstetrics & gynecology clerkship. New York: McGraw-Hill, Medical Pub. Division. ص. 100. ISBN:0-07-144874-8.
- ^ Ghosh, Amit K. (2008). Mayo Clinic Internal Medicine Review: Eighth Edition (Mayo Clinic Internal Medicine Review). Informa Healthcare. ص. 55. ISBN:1-4200-8478-X.
- ^ British Journal of Anaesthesia: "Primary pulmonary hypertension in pregnancy; a role for novel vasodilators" March 19, 2011 نسخة محفوظة 18 يونيو 2016 على موقع واي باك مشين.
| في كومنز صور وملفات عن: فرط ضغط الدم الرئوي |