|
تضامنًا مع حق الشعب الفلسطيني |
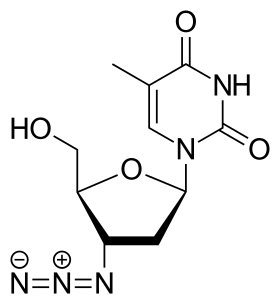
زيدوفودين
| زيدوفودين | |
|---|---|
| الاسم النظامي | |
| 1-[(2R,4S,5S)-4-Azido-5-(hydroxymethyl)oxolan-2-yl]-5-methylpyrimidine-2,4-dione[1] | |
| اعتبارات علاجية | |
| اسم تجاري | Retrovir |
| ASHPDrugs.com | |
| فئة السلامة أثناء الحمل | B3 (أستراليا) C (الولايات المتحدة) |
| طرق إعطاء الدواء | عبر الفم، عبر المستقيم، عبر الحقن الوريدي |
| بيانات دوائية | |
| توافر حيوي | إمتصاص كامل, حسب إستقلاب المرور الأول ،التوافر الدموي % 75 |
| ربط بروتيني | 30 إلى 38% |
| استقلاب (أيض) الدواء | عبر الكبد |
| عمر النصف الحيوي | 0.5 إلى 3 ساعات |
| إخراج (فسلجة) | عبر البول، عبر البراز |
| معرّفات | |
| CAS | 30516-87-1 |
| ك ع ت | J05J05AF01 AF01 |
| بوب كيم | CID 35370 |
| درغ بنك | DB00495 |
| كيم سبايدر | 32555 |
| المكون الفريد | 4B9XT59T7S |
| ChEBI | CHEBI:10111 |
| ChEMBL | CHEMBL129 |
| NIAID ChemDB | 000001 |
| بيانات كيميائية | |
| الصيغة الكيميائية | C10H13N5O4 |
| الكتلة الجزيئية | 267.242 g/mol |
| تعديل مصدري - تعديل | |
زيدوفيدين (ZDV)(التسمية الدولية المشتركة) أو أزيدوتيميدين (AZT) هو دواء مضاد للفيروسات القهقرية يستعمل في علاج داء فقدان المناعة المكتسبة AIDS الناتج عن الإصابة بفيروس العوز المناعي البشري HIV.
زيدوفيدين هو من مثبطات أنزيم المنتسخة العكسية النوكليوزيدية التي تمنع عملية النسخ العكسي أي تمنع تركيب الحمض النووي الريبوزي المنقوص الأكسجين (الدنا DNA) الفيروسي انطلاقا من الحمض الريبوزي النووي (الرنا RNA) الفيروسي.
كان الزيدوفيدين أول بارقة أمل لعلاج الأيدز، إذ استطاع تخفيض سرعة تكاثر الفيروس لدى المصابين بشكل ملحوظ بالإضافة إلى تحسنات سريرية ومناعية.[2] وقد وافقت عليه إدارة الغذاء والدواء الأمريكية (US FDA) كأول دواء لعلاج الأيدز سنة 1987.[3]
تاريخ
تم تركيب الزيدوفيدين لإول مرة سنة 1964 بواسطة Jerome Horwitz التابع لمعهد السرطان Barbara Ann Karmanos و لكلية الطب في جامعة ولاية وين، بمنحة من معهد الصحة الوطنية الأمريكية.[4][5][6] لكن تم التخلي عن تطوير الدواء بسبب خموله بيولوجيا عند الفئران.[4][7]
في سنة 1974، بين Wolfram Ostertag، من معهد Max Planck في ألمانيا، على قدرة الزيدوفين في مواجهة فيروس الصديق Friend virus ( نوع من أنواع الفيروسات التي تسبب سرطان الدم عند الفئران) الفيروسات القهقرية عند الفئران.[8]
نجاح العلاج
في ماي 1984، وبعد وقت قصير من التأكد أن فيروس HIV هو المسؤول عن الإصابة بداء فقدان المناعة المكتسبة، أطلق Hiroaki Mitsuya ،Samuel Broder و Robert Yarchoan من المعهد الوطني للسرطان(National Cancer Institute-NCI ) بالولايات المتحدة الأمريكية، أطلقو برنامج لتطوير علاجات ضد HIV/AIDS.[9] باستعمال نسل خلوي من الخلايا اللمفاوية التائية -T-المساعدة (خلايا 4+CD أو خلايا TH)، طور علماء NCI اختبار لاختيار الأدوية حسب قدرتها على حماية خلايا +CD من الموت بسبب فيروس HIV.[10]
بقيت مادة الزيدوفيدين غير مستعملة إلى حدود فبراير من سنة 1985 حيث قام مجموعة من الباحثين التابعين للمعهد الوطني للسرطان رفقة باحثين تابعين لشركة Burroughs-Wellcome الصيدلانية (حالياغلاكسو سميث كلاين GSK-GlaxoSmithKline) بإجراء اختبارات على هذا الدواء بهدف إيجاد علاج لداء فقدان المناعة المكتسبة. بعد أن بين الباحثون فعالية الزيدوفيدين على نشاط أنزيم المنتسخة العكسية في المختبر [11] ، أنجز الفريق أول اختبار سريري الذي بين ان اللزيدوفيدين بزيد من عدد خلايا +CD4 عند المصابين بالسيدا .
مكنت تجربة عشوائية للزيدوفيدين مع دواء وهمي لمدة 24 أسبوع بجرعة 1500 ملغ في اليوم من إستنتاج قدرة الزيدوفيدين على إطالة أمد الحياة بالنسبة للمصابين بداء السيدا [12]. هده التجربة أشرفت عليها شركة Burroughs-Wellcome و قد مكنتها من تقديم براءة اختراع AZT سنة 1985، بعد سنتين وفي 20 مارس 1987 وافقت FDA (إدارة الغذاء والدواء الأمريكية) على مادة AZT كدواء يمكن إستعماله في علاج الإصابة بفيروس نقص المناعة المكتسبة والسيدا.[13] الوقت الفاصل بين البرهنة على فعالية AZT ضدد فيروس HIV في المختبر وبين حصول الدواء على الترخيص كان هو 25 شهرا ويعتبر بذلك أقصر وقت حصول على الترخيص بالنسبة لدواء في التاريخ الحديث.
الجرعة التي كانت مستعملة في بدايات العلاج ب AZT كانت 2400 ملغ في اليوم (6 جرعات) و هي الجرعة المستنتجة من دراسة Mitsuya و فريقه التابعين ل NCI التي أكدت انها ضرورية لوقف نشاط النسخ العكسي للفيروس.[11] العلاجات الحالية تستعمل جرعات اٌقل ك 300 ملغ في اليوم (2 أو 3 جرعات)
دراسات جديدة أكدت فعالية AZT في العلاج المبكر بالنسبة للمصابين الدين لا يضهرون أعراض مع عدد خلايا لمفاوبة +CD4 أقل من 500 خلية في الملمتر المكعب من الدم CD+ <500/mm³.[14]
العلاجات الأحادية المبكرة ب AZT كانت محور دراسة فرنسية-إنجليزية سنة 1993 عرفت باسم 'كونكورد Concorde' [15]، الدراسة قارنت بين اختيارين علاجيين باعتماد AZT ; الأول مبكر والثاني غير مبكر على امتداد 3 سنوات وقد وضعت في موضع الشك فعالية وفائدة تناول AZT في العلاج الأحادي المبكر .
ابتداء من سنة 1996 أصبح العلاج بالزيدوفيدين وباقي مضادات الفيروسات القهقرية يعطى مع جزيئات وأدوية أخرى في إطار العلاج الثلاثي للأيدز [16] · .[17]
تركيب
AZT أو أزيدوتيميدين هو مركب شبيه للتيميدين حيث تم استبدال المجموعة الكحولية (-OH) على مستوى الكربون رقم '3 من سكر الريبوز منقوص الأوكسجين أو ديزوكسيريبوز بمجموعة أزيدية . و قد نجح في تركبيه Jerome Horwitz عام 1964 انطلاقا من التيميدين[5]

آلية العمل
كباقي مثبطات أنزيم المنتسخة العكسية يقوم AZT بمنع عملية النسخ العكسي التي تمكن الفيروس من إنتاج الحمض النووي الريبوزي المنقوص الأكسجين دنا (DNA) انطلاقا من الحمض الريبوزي النووي رنا (RNA) و بذلك ينمع اندماج DNA الفيروس في DNA الخلية البشرية المصابة وتعبيره وتكاثره -عندما يندمج الحمض النووي الفيروسي مع الحمض النووي الخلوي تسمى الخلية «بروفيروس Provirus».[18][19][20]
تقوم المجموعة الأزيدية بزيادة خاصية الذوبانية في الذهنيات للزيدوفيدين مما يمكنه من عبور الغشاء السيتوبلازمي للخلايا بسهولة بواسطة ظاهرة الإنتشار و كذلك عبور الحاجز الدموي الدماغي (Blood-Brain Barrier).
جُزيئة AZT هي غير فعالة بحد ذاتها إلا بعد تحويلها إلى شكلها الفعال، هذا التحويل المََُفَعِل يكون بواسطة أنزيم الكيناز (Kinase Enzyme) الذي يقوم بفَسْفَرَةِ AZT عبر إلصاق مجموعة ثلاثي الفوسفاط (TriPhosphate)في الكربون رقم '5 من سكر الريبوز منقوص الأوكسجين ليصبح أزيدوتيميدين-'5-ثلاثي فوسفاط (AZT-5'-TriPhosphate)
AZT هو شبيه نيكليوزيدي يتحول بعد الفسفرة إلى شبيه نيكليوتيدي، خلال عملية النسخ العكسي يخلط أنزيم المنتسخة العكسية الفيروسي بين النيكليوتيدات الطبيعية الخلوية وبين أشباه النيكليوتيدات كالزيدوفيدين فيستعملها من أجل تركيب الحمض النووي الفيروسي، لكن وبسبب غياب المجموعة الكحوليه (OH) على مستوى الكربون '3 تتوقف عملية التركيب وبالتالي تكاثر الفيروس [21] · .[22][23]
الإستقلاب
يتخلص الجسم من الزيدوفيدين عبر الإستقلاب الكبدي أساسا، المركب الأهم الناتج عن هذه العملية هو GZDV من (Azido-3-deoxy-5-O-b -D-Glucopyranuronosylthymidine ) الذي يتميز بخاصية اطراح عبر البول 3 مرات أكثر من AZT غير المستقلب.
مركب آخر ناتج عن هذه العملية هو AMT أي (3'-amino-3'-deoxythymidine) و الذي له خاصية طرح عبر البول 5 مرات أقل من AZT.[24]
التأثيرات الجانبية
بالنسبة للتأيرات الجانية يعتبر فقر الدم أهمها، حيث عانا منه المصابين خلال تجارب AZT مما فرض إعادة تقيم لنسبة الاضرار بالمقارنة مع الفوائد، لكن وبسبب غياب أي علاج آخر للأيدز خلال تلك فترة، كانت تعتبر الإصابة بالفيروس أخطر من التأثيرات الجانبية للدواء في بداية التسعينات.
أهم التأثيرات الجانبية للزيدوفيدين هي : دوار، صداع الرأس، تحريك الشحوم، اختفاء صبغة الأظافر هناك تأثيرات جانبية أخطر وهي فقر الدم هذه التأتيرات يمكن أن تكون ناتجة عن حساسية أنزيم بوليميراز الدنا γ-ADN بوليميراز ( γ-DNA Polymerase ) في ميتوكوندريات الخلية
بالإضافة إلى عمله الكابح لأنزيم المنتسخة العكسية الفيروسي يستطيع الشكل الفعال من الزيدوفيدين (أي أزيدوتيميدين-'5-ثلاثي فوسفاط ) كبح نشاط أنزيم بوليميراز الدنا البشري الضروري للانقسام الخلوي للخلايا السليمة، لكن للزيدوفيدين قابلية 100 إلى 300 مرة أكبر لأنزيم المنتسخة العكسية البشري منه من أنزيم بوليميراز الدنا البشري الشيء الذي يفسر نشاطه المضاد للفيروسات نوع خاص من أنزيم بوليميراز الدنا و هو مسؤول عن مضاعفة الحمض النووي في الميتوكندريات، له حساسية نسبيا أكبر للكبح بواسطة AZT ما يفسر سميته تجاه بعض الخلايا.[21] وقد تم أيضا تبين ان AZT يرفع من مستوى الأكسدة الخلوية في بعض الخلايا.
المقاومة الفيروسية
رغم أن المصاب قادر على تحمل جرعات كبيرة من الزيدوفيدين إلا أنها غير قادرة على منع تكاثر الفيروس بصفة نهائية، فالزيدوفيدين ينقص فقط من سرعة التكاثر ويبطء من تقدم المرض يستطيع فيروس HIV تطوير مقاومة ضدد الدواء خلال فترات العلاج الطويلة بالزيدوفدين بواسطة طفرة في الجينات المسؤولة عن إنتاج أنزيم المنتسخة العكسية . وقصد تجنب تطوير المقاومة ضدد الدواء ينصح الأطباء بأخد دواء آخر مضاد لأنزيم المنتسخة العكسية رفقة AZT بالإضافة إلى مضاد فيروسي آخر من مجموعة أخرى كمضادات تجميع البروتينات الفيروسية أو مضاد منتسخة عكسية غير نيكليوزيدي . هذا النوع من العلاج يطلق عليه اسم 'HAART' اختصارا ل (Highly Active Anti Retroviral Therapy) أي العلاج المضاد للفيروسات عالي النشاط
خصائص الزيدوفيدين المؤكسدة
دراسات عديدة اتبثت ان الزيدوفيدين يؤكسد الميتوكوندريات [25] · [26]، عبر الرفع من مستوى بيروكسيد الهيدروجين في البلعميات الكبرى.[27]
AZT قد يكون سبب في تكوين البيروكسينيتريت (PeroxyNitrites).[28] و يتسبب في أكسدة الحمض النووي الخاص بالميتوكوندريات ,لكن تمكن مضاادات الأكسدة (كفيتامين C وفيتامين E) من تجنب هذه الأكسدة.[25] هذه الخصائص المؤكسدة للزيدوفيدين تمت البرهنة عليها مختبريا بواسطة Handlon و فريقه.[29]
التداخلات الدوائية
يعمل الزيدوفيدين بتعاون مع باقي الأدوية المضادة ل HIV, لكن دواء أسيكلوفير (Aciclovir) و ريبافيرين (Ribavirine) يتسببان في ينقص فعالية الزيدوفيدين الأدوية التي تمنع الإستقلاب الكبدي للزيدوفيدين، كالأسبرين (حمض أستيل ساليسيليك), أيندوميتاسين وتريميتوبريم تنقص نسبة طرح AZT و ترفع من سميته.[30]
انتقادات
كان دواء الزيدويدين موضع عدة انتقادات بسبب ثمنه، الطريقة التي تم بها الحصول على براءة الاختراع [31] و بسبب عدم الثقة التي طورها ضده Peter Duesberg في نقده لفرضية الانتساخ العكسي للإيدز
الثمن
تم تسويق AZT في الولايات المتحدة الأمريكية بثمن 10000 دولار للسنة من العلاج,[32][33] هذا الثمن أدى إلى تأجيج غضب المصابين وتكوين حركة Act Up الاحتجاجية [34] التي نظمت أولى مظاهراتها أمام بورصة نيويورك في شارع وول ستريت.[33]
سنة 1989, وبعد انتهاء التجربة "ACTG 019" التي أدت إلى زيادة مهمة في عدد المصابين اللذين يعالجون ب AZT و بالتالي ارتفاع أرباح شركة Burroughs-Wellcome للصيدلانيات، قام مناضلون من حركة Act Up بعملية كوموندو في وول ستريت أدت إلى وقف التعاملات في البورصة قصد إثارة انتباه وسائل الإعلام[6] · .[35] نتيجة لذلك تم إستدعاء,T.E. Haigler, رئيس شركة Burroughs-Wellcome , إلى جلسة استماع بالكونغرس الأمريكي قصد شرح سبب ارتفاع ثمن AZT,[32] قبل أن يخفض ثمنه بعد مرور وقت قصير وإنخفض ثمن العلاج أيضا نتيجة تخفيض الجرعات.[32]
النقاش حول ثمن AZT و باقي مضادات الفيروسات القهقرية طفى إلى السطح من جديد مع ظهور العلاج الثلاثي ومشكل الوصول إليهم في البلدان الفقيرة
براءة الاختراع
سنة 1992, قامت جمعية (Public Citizen) الأمريكية برفع دعوى قضائية لطلب إلغاء براءة اختراع AZT, لكن محكمة الإستئناف الأمريكية فصلت في القضية لصالح Burroughs-Wellcome الشركة المالكة لبراءة الاختراع[36] · .[37] في سنة 2002 رفعت مؤسسة (AIDS Healthcare Foundation) دعوى قضائية أخرى ضدد براءة الاختراع، لكن مدة صلاحية البراءة انتهت سنة 2005 مما سمح لشركات الصناعات الصيلادنية الأخرى بصنع أدوية جنيسة للزيدوفيدين وافقت FDA على أربع أشكال جنيسة منها.
موقف بيتر ديسبرغ
يزعم الدكتور Peter Duesberg أن AZT و باقي المواد المزيلة للمناعة (كوكايين , أمفيتامين , نيتريت ... إلخ) هي المسؤولة عن الإيدر أكثر من فيروس HIV في البلدان الغربية.[38] يعتبر أغلب العلماء ان هده الفرضية غير معقولة نظرا لكثرة المعطيات السريرية والوبائية الموثوق فيها التي تعارضها,[39] خصوصا الانخفاض الكبير في عدد الحالات ونسبة الوفاة المترتبة عن ذلك المقرون باستعمال AZT في العلاج الثلاثي خلال الفترة ما بين 1995 و 1997 (انخفاض بنسبة %70 في سنتين).[40]
المراجع
- ^ "Zidovudine". PubChem Public Chemical Database. NCBI. مؤرشف من الأصل في 2014-02-22. اطلع عليه بتاريخ 2011-04-10.
- ^ PMID 3463865 (ببمد: 3463865)
Citation will be completed automatically in a few minutes. Jump the queue or expand by hand - ^ "U.S Approves Drug to Prolong Lives of AIDS Patients". New York Times. 21 مارس 1987. مؤرشف من الأصل في 2018-08-04.
- ^ أ ب PMID 20018391 (ببمد: 20018391)
Citation will be completed automatically in a few minutes. Jump the queue or expand by hand - ^ أ ب Horwitz، JP (1964). "The monomesylates of 1-(2-deoxy-bd-lyxofuranosyl) thymines". Org. Chem. Ser. Monogr. ج. 29 ع. 7: 2076–9. DOI:10.1021/jo01030a546.
{{استشهاد بدورية محكمة}}: الوسيط author-name-list parameters تكرر أكثر من مرة (مساعدة) - ^ أ ب Detours V; Henry D (writers/directors) (2002). I am alive today (history of an AIDS drug) (Film). ADR Productions/Good & Bad News.
- ^ "A Failure Led to Drug Against AIDS". نيويورك تايمز. 20 سبتمبر 1986. مؤرشف من الأصل في 2009-08-16. اطلع عليه بتاريخ 2010-06-30.
- ^ Ostertag، W.؛ Roesler، G.؛ Krieg، C. J.؛ Kind، J.؛ Cole، T.؛ Crozier، T.؛ Gaedicke، G.؛ Steinheider، G.؛ Kluge، N.؛ Dube، S. (1974). "Induction of endogenous virus and of thymidine kinase by bromodeoxyuridine in cell cultures transformed by Friend virus". Proceedings of the National Academy of Sciences of the United States of America. ج. 71 ع. 12: 4980–4985. Bibcode:1974PNAS...71.4980O. DOI:10.1073/pnas.71.12.4980. PMC:434023. PMID:4531031.
- ^ NIH Clinical Center's 50th Anniversary. http://www.cc.nih.gov/about/news/anniver50/_pdf/CC_50th_Anniversary_Celebration.pdf نسخة محفوظة 19 يونيو 2013 على موقع واي باك مشين.
- ^ Mitsuya H, Weinhold K, Furman P, St Clair M, Li, Lars, Lehrman S, Gallo R, Bolognesi D, Barry D, Broder S (1985). "3'-Azido-3'-deoxythymidine (BW A509U): an antiviral agent that inhibits the infectivity and cytopathic effect of human T-lymphotropic virus type III/lymphadenopathy-associated virus in vitro". Proc Natl Acad Sci USA. ج. 82 ع. 20: 7096–100. Bibcode:1985PNAS...82.7096M. DOI:10.1073/pnas.82.20.7096. PMC:391317. PMID:2413459.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ أ ب [1] 3'-Azido-3'-deoxythymidine (BW A509U) : An Antiviral Agent That Inhibits the Infectivity and Cytopathic Effect of Human T-Lymphotropic Virus Type III/Lymphadenopathy-Associated Virus in vitro ; Hiroaki Mitsuya, Kent J. Weinhold, Phillip A. Furman, Marty H. St. Clair, Sandra Nusinoff Lehrman, Robert C. Gallo, Dani Bolognesi, David W. Barry, and Samuel Broder ; PNAS 1985;82;7096-7100 "نسخة مؤرشفة" (PDF). مؤرشف من الأصل في 2007-09-30. اطلع عليه بتاريخ 2014-06-03.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ [2] The efficacy of azidothymidine (AZT) in the treatment of patients with AIDS and AIDS-related complex. A double-blind, placebo-controlled trial ; Fischl MA, Richman DD, Grieco MH, Gottlieb MS, Volberding PA, Laskin OL, Leedom JM, Groopman JE, Mildvan D, Schooley RT ; N Engl J Med. 1987 Jul 23;317(4):185-91. "نسخة مؤرشفة". مؤرشف من الأصل في 2012-05-10. اطلع عليه بتاريخ 2019-12-07.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ Cimons، Marlene (21 مارس 1987). "U.S. Approves Sale of AZT to AIDS Patients". Los Angeles Times. ص. 1.
- ^ نشر نتائج التجربة السريرية الأمريكية ACTG 019 سنة 1989 : Volberding PA. Lagakos SW, Koch MA قالب:Et al. « Zidovudine in asymptomatic human immunodeficiency virus infection : a controlled trial in persons with fewer than 500 CD4-positive cells per cubic millimeter » N Engl J Med. 1990 ; 322:941-9.
- ^ (بالإنجليزية) Concorde Coordinating Committee. « Concorde : MRC/ANRS randomised double-blind controlled trial of immediate and deferred zidovudine in symptom-free HIV infection » Lancet 1994 ; 343:871-81.
- ^ (بالإنجليزية) De Clercq ECatégorie:Utilisation du paramètre auteur dans le modèle article, « HIV resistance to reverse transcriptase inhibitors. », في Biochem Pharmacol, vol. 47, no 2, 1994, ص. 155-69
- ^ (بالإنجليزية) Yarchoan R, Mitsuya H, Broder SCatégorie:Utilisation du paramètre auteur dans le modèle article, « AIDS therapies. », في Sci Am, vol. 259, no 4, 1988, ص. 110-9
- ^ Mitsuya H, Weinhold K, Furman P, St Clair M, Lehrman S, Gallo R, Bolognesi D, Barry D, Broder S (1985). "3'-Azido-3'-deoxythymidine (BW A509U): an antiviral agent that inhibits the infectivity and cytopathic effect of human T-lymphotropic virus type III/lymphadenopathy-associated virus". Proc Natl Acad Sci USA. ج. 82 ع. 20: 7096–100. Bibcode:1985PNAS...82.7096M. DOI:10.1073/pnas.82.20.7096. PMC:391317. PMID:2413459.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Yarchoan R, Klecker R, Weinhold K, Markham P, Lyerly H, Durack D, Gelmann E, Lehrman S, Blum R, Barry D (1986). "Administration of 3'-azido-3'-deoxythymidine, an inhibitor of HTLV-III/LAV replication, to patients with AIDS or AIDS-related complex". Lancet. ج. 1 ع. 8481: 575–80. DOI:10.1016/S0140-6736(86)92808-4. PMID:2869302.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Mitsuya H, Yarchoan R, Broder S (1990). "Molecular targets for AIDS therapy". Science. ج. 249 ع. 4976: 1533–44. Bibcode:1990Sci...249.1533M. DOI:10.1126/science.1699273. PMID:1699273.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ أ ب (بالإنجليزية) Mitsuya H, Weinhold K, Furman P, St Clair M, Lehrman S, Gallo R, Bolognesi D, Barry D, Broder SCatégorie:Utilisation du paramètre auteur dans le modèle article, « 3'-Azido-3'-deoxythymidine (BW A509U) : an antiviral agent that inhibits the infectivity and cytopathic effect of human T-lymphotropic virus type III/lymphadenopathy-associated virus in vitro. », في Proc Natl Acad Sci U S A, vol. 82, no 20, 1985, ص.
7096-100 [النص الكامل] نسخة محفوظة 8 مايو 2006 على موقع واي باك مشين. "نسخة مؤرشفة". مؤرشف من الأصل في 2006-05-08. اطلع عليه بتاريخ 2014-06-03.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ (بالإنجليزية) Yarchoan R, Klecker R, Weinhold K, Markham P, Lyerly H, Durack D, Gelmann E, Lehrman S, Blum R, Barry DCatégorie:Utilisation du paramètre auteur dans le modèle article, « Administration of 3'-azido-3'-deoxythymidine, an inhibitor of HTLV-III/LAV replication, to patients with AIDS or AIDS-related complex. », في Lancet, vol. 1, no 8481, 1986, ص. 575-80
- ^ Cette vidéo montre une modélisation 3D illustrant le mode d'action de l'AZT[وصلة مكسورة] نسخة محفوظة 03 مارس 2016 على موقع واي باك مشين.
- ^ RXLIST Pharmacocinétique de l'AZT نسخة محفوظة 07 سبتمبر 2008 على موقع واي باك مشين.
- ^ أ ب AZT Treatment Induces Molecular and Ultrastructural Oxidative Damage to Muscle Mitochondria José García de la Asunción, Maria L. del Olmo, Juan Sastre, Arantxa Millán, Antonio Pellín, Federico V. Pallardó and José Viña ; J. Clin. Invest. Volume 102, Number 1, July 1998, 4–9 نسخة محفوظة 30 يونيو 2020 على موقع واي باك مشين.
- ^ Azidothymidine causes functional and structural destruction of mitochondria, glutathione deficiency and HIV-1 promoter sensitization[وصلة مكسورة] ; Tokio Yamaguchi, Iyoko Katoh and Shun-ichi Kurata ; Eur. J. Biochem. 269, 2782-2788 (2002) نسخة محفوظة 2022-02-09 على موقع واي باك مشين.
- ^ Azidothymidine promotes free radical generation by activated macrophages and hydrogen peroxide-iron-mediated oxidation in a cell-free system. نسخة محفوظة 05 مارس 2016 على موقع واي باك مشين.
- ^ Role of reactive oxygen species and poly-ADP-ribose polymerase in the development of AZT-induced cardiomyopathy in rat. نسخة محفوظة 3 فبراير 2020 على موقع واي باك مشين.
- ^ Thiol reduction of 3'-azidothymidine to 3'-aminothymidine : kinetics and biomedical implications. نسخة محفوظة 05 مارس 2016 على موقع واي باك مشين.
- ^ Zidovudine sur medecinenet.com نسخة محفوظة 26 يوليو 2017 على موقع واي باك مشين.
- ^ The Best Democracy Money Can Buy par Greg Palast (2002)
- ^ أ ب ت Peter Arno, Against the Odds : The Story of AIDS Drug Development, Politics And Profits, 1992, HARPERCOLLINS. ISBN 0-06-018309-8.
- ^ أ ب Histoire scientifique, commerciale et politique de l'AZT racontée par ses principaux protagonistes dans le film documentaire SIDA, une histoire de l'AZT (2002) de Vincent Detours et دومينيكو هنري . نسخة محفوظة 03 مارس 2016 على موقع واي باك مشين.
- ^ ACT UP New York: Capsule History, Actupny.org نسخة محفوظة 24 ديسمبر 2017 على موقع واي باك مشين.
- ^ YouTube (مقطع من وثائقي SIDA, une histoire de l'AZT (2002)). نسخة محفوظة 6 أبريل 2016 على موقع واي باك مشين.
- ^ People with Aids Health Group v. Burroughs Wellcome Co., 1992 U.S. Dist. LEXIS 578
- ^ US Court of Appeals fot the Federal Circuit. University of Houston -- Health Law and Policy Institute (المحرر). "Burroughs Wellcome Co. v. Barr Laboratories, 40 F.3d 1223 (Fed. Cir. 1994)". مؤرشف من الأصل في 2016-12-23. اطلع عليه بتاريخ 2007-02-28.
{{استشهاد ويب}}:|محرر=باسم عام (مساعدة) - ^ (بالإنجليزية) Duesberg P, Koehnlein C, Rasnick DCatégorie:Utilisation du paramètre auteur dans le modèle article, « The chemical bases of the various AIDS epidemics : recreational drugs, anti-viral chemotherapy and malnutrition. », في J Biosci., vol. 28, no 4, 2003, ص. 383-412 [النص الكامل]
- ^ "The Evidence That HIV Causes AIDS". مؤرشف من الأصل في 2009-01-17. اطلع عليه بتاريخ 2006-03-29.
- ^ San Francisco AIDS Incidence, Mortality and prevalence by year, 1980-2001 نسخة محفوظة 2 فبراير 2020 على موقع واي باك مشين.
| زيدوفودين في المشاريع الشقيقة: | |