|
تضامنًا مع حق الشعب الفلسطيني |
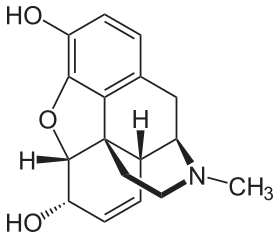
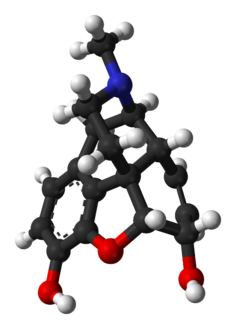
مورفين
المورفين (الاسم الدولي غير مسجّل الملكية)، يُسوّق تحت العديد من الأسماء التجارية، هو مسكّن ألم قوي من فئة الأفيونيات. يعمل المورفين بشكل مباشر على الجهاز العصبي المركزي لتقليل الشعور بالألم. يمكن استخدامه لكل من الألم الحاد والألم المزمن. كثيرًا ما يستخدم المورفين كذلك لتخفيف الألم الناجم عن انسداد العضلة القلبية وكذلك خلال الولادة. يمكن إعطاؤه عن طريق الفم، أو العضل، أو تحت الجلد، أو عن طريق الوريد، أو إلى الفراغ حول النخاع الشوكي، أو عن طريق المستقيم.[3] عند إعطاء المورفين عن طريق الوريد يكون التأثير الأقصى بعد 20 دقيقة، أما عند تناوله عن طريق الفم فيكون التأثير الأقصى بعد 60 دقيقة ويبقى مفعوله ما بين 3 و7 ساعات.[3][4] هناك أيضًا تركيبات مورفين مديدة المفعول.[3]
تشمل الآثار الجانبية الخطيرة التي قد تنجم من المورفين انخفاض التنفس وانخفاض ضغط الدم. للمورفين احتمال مرتفع أن يؤدي للإدمان عليه وإساءة الاستعمال. إذا تم تخفيض الجرعة بعد فترة طويلة من الاستخدام قد تظهر عوارض الانسحاب من المواد الأفيونية. وتشمل الآثار الجانبية الشائعة النعاس، والتقيؤ، والإمساك. وينصح الحذر عند استخدام المورفين أثناء الحمل أو الإرضاع حيث يؤثر المورفين على الأطفال.[3]
استُخلص المورفين للمرة الأولى بين عام 1803 وعام 1805 على يد الصيدلي الألماني فريدريك سيرتونر.[5][6] وعمومًا يُعتقد أنها كانت المرة الأولى التي تُعزل بها مادة فعالة من النبات.[7] بدأت شركة ميرك تسويقه تجاريًا في عام 1827.[5] وقد استُخدم المورفين على نطاق واسع بعد اختراع محقنة تحت الجلد في 1853-1855.[5][8] أطلق سيرتونر بداية الاسم مورفيوم وفقًا للإله الأحلام الإغريقي، مورفيوس، بسبب الميل للنوم عند تناوله.[8][9]
المصدر الرئيسي للمورفين هو عزل نبات الخشخاش المنوم من قش الخشخاش.[10] في عام 2013 تم إنتاج ما يقارب الـ 523,000 كيلوغرام من المورفين.[11] استُخدم منها حوالي 45,000 كيلوغرام لعلاج مباشر للألم، مما يشكّل ارتفاع الكمية بأربعة أضعاف خلال عقدين من الزمن.[11] معظم استهلاك المورفين لهذا الغرض كان في دول العالم المتقدّم.[11] يُستخدم 70% من المورفين لصناعة مواد أفيونية أخرى مثل الهيدرومورفين، والأوكسيكودون، والهيروين، والميثادون.[11][12][13] إن المورفين دواء في الجدول الثاني في الولايات المتحدة،[12] في الفئة (أ) في المملكة المتحدة،[14] والجدول الأول في كندا.[15] يتواجد كذلك المورفين في قائمة منظمة الصحة العالمية للأدوية الأساسية، قائمة بأهم الأدوية الضرورية في نظام رعاية صحية أساسي.[16]
استخداماته الطبية
يُستخدم المورفين في المقام الأول لعلاج كل من الألم الشديد الحاد والمزمن. كما ويستخدم لعلاج الألم الناتج عن انسداد العضلة القلبية وآلام الولادة.[17] ومع ذلك، توجد مخاوف من أن المورفين قد يزيد معدّل الوفيات في انسداد عضلة القلب غير المرتبط بمقطع ST.[18] يُستخدم المورفين كذلك بشكل تقليدي في علاج وذمة الرئة الحادة.[17] مع ذلك، في مراجعة أُجريت عام 2006 وجدوا أدلة قليلة فقط تدعم هذه الممارسة.[19]
أستخدم المورفين في البداية كمادة مسكنة لكن ثبت بعد ذلك أنه يمكن أن يسبب الإدمان. وهو له أيضًا العديد من الآثار الجانبية مثل احتباس البول، قيء، انخفاض في ضغط الدم، زيادة الهيستامين مما يؤدي إلى حساسية، وطمس المركز التنفسي مما يؤدي إلى الوفاة [20]، وتقليل حركة الأمعاء مما يؤدي إلى الإمساك.
لا يجب استخدام المورفين كمسكن في حالات الولادة حيث أنه يعبر المشيمة مما يؤدي إلى اختناق الجنين Neonatal Asphyxia، الأزمات الصدرية، إصابات الدماغ، في حالة المغص المراري يجب دمجه مع الاتروبين Atropine.
في حالة التسمم بالمورفين يتم عمل غسيل معدة أو أعطاء محثات قيء. يمكن أيضًا إعطاء نالوكسون
موانع الاستعمال
تشمل موانع الاستعمال النسبية للمورفين:
- هبوط في التنفس عندما لا تتواجد المعدات الملائمة.[3]
- على الرغم من أنه قد اعتُقد سابقًا أن استعمال المورفين ممنوعًا في التهاب البنكرياس الحاد، إلا أن مراجعة للأبحاث لم تظهر أي دليل لذلك.[21]
أعراض جانبية
إمساك
يعمل المورفين، مثل اللوبيراميد وغيره من المواد الأفيونية، على الضفيرة العضليّة المعويّة في الأمعاء، فيحدّ من حركة الأمعاء، مما يسبّب الإمساك. إن آثار المورفين على الجهاز الهضمي هي بالمقام الأول عن طريق مستقبلات μ-الأفيونية في الأمعاء. يقلل المورفين نسبة العبور المعوي عن طريق تثبيط إفراغ المعدة وتقليل التمعّج الدافع للأمعاء. كذلك الانخفاض في الإفرازات المعوية وزيادة امتصاص السوائل المعوية تساهم في أثر الإمساك. قد تعمل المواد الأفيونية أيضًا بشكل غير مباشر من خلال تشنجات معوية توترية بعد تثبيط توليد أكسيد النتريك.[22] وأظهرت الدراسات أن هذا التأثير في الحيوانات حيث عكس نظير أكسيد النتريك، ل-أرجنين، التغييرات التي يسببها المورفين لحركة الأمعاء.[23]
اختلال التوازن الهرموني
تشير الدراسات السريرية باستمرار أن المورفين، مثل المواد الأفيونية الأخرى، غالبًا ما يسبب قصور الغدد التناسلية واختلال التوازن الهرموني في المستخدمين المزمنين من كلا الجنسين.
تأثيرات على الأداء البشري
تستخلص معظم الدراسات أن المواد الإفيونية تؤدي إلى تأثير منخفض جدًا على أداء الإنسان في الاختبارات الحسية، والحركية، والقدرة على الانتباه.
تأثيره على الإنسان
تأثير المورفين يكون بصفة أساسية على الجهاز العصبي المركزي فيؤدي إلى الهدوء والنوم وتسكين الألم وهو مثبط (يقلل النشاط) لمركز التنفس والسعال ولمركز تنظيم الحرارة مما يؤدي إلى الهدوء والنوم وتسكين الألم وخفض حرارة الجسم، وكلها أعراض مباشرة للتثبيط الذي يصيب الجهاز العصبي. وللمورفين بعض التأثيرات المنشطة لبعض مناطق الجهاز العصبي ويظهر ذلك في صورة غثيان وقيء وضيق حدقة العين وهبوط في سرعة نبض القلب. ولكن الكميات المفرطة منه تسبب كبحا لوظائف الجهاز العصبي مما يسبب ضيق تنفس وسعال شديد.
استخلاصه
هو مجرد مادة من أشباه القلويات من عشرين مادة يمكن استخراجها من الخشخاش وقد تم بعد ذلك تركيبه صناعيا في صورة نقية.
التسمم الحاد بالمورفين
يحدث نتيجة تعاطي جرعات زائدة، سواءً أثناء العلاج أو بغرض الانتحار أو أثناء تعاطيه كعقار للإدمان. الأعراض: تظهر بعد نصف ساعة إذا تم تناول العقار عن طريق الفم، وبعد دقائق إذا تم تناول العقار عن طريق الحقن، وهي تتجلى في صورة سبات (غيبوبة) مع ضعف في التنفس كما ينخفض ضغط الدم ويبطأ النبض مع قوته ويشحب الجلد مع زيادة إفراز العرق وتضيق حدقة العين بدرجة كبيرة فتصبح في حجم رأس الدبوس وينتهي الأمر بالوفاة نتيجة شلل المراكز العصبية وخاصة مركز التنفس.
المورفين طليعة الأفيونات الأخرى
طليعة دوائية
يُعد المورفين المركب الطليعي في تصنيع عدد من الأفيونات مثل ثنائي هيدرومورفين والهيدرومورفين والأوكسيكودين والكودين الذي يُشتق منه وحده عائلة كبيرة من الأدوية شبه الاصطناعية.[24]
طليعة المركبات غير الشرعية
يُنتج المورفين غير الشرعي -رغم ندرته- من الكودين المتوافر في الأسواق دون الحاجة إلى وصفة طبية في أدوية السعال ومسكنات الألم. يمثل المورفين المستخرج من منتجات المورفين مديدة التحرر مصدرًا محظورًا آخر للمورفين غير الشرعي. يمكن الاعتماد على التفاعلات الكيميائية لتحويل المورفين وثنائي هيدرومورفين والهيدروكودون تاليًا إلى الهيروين أو الأفيونات الأخرى ]مثل ثنائي أسيتيل ثنائي هيدرومورفين (بارالودين) والثيباكون[.[25]
يحتاج تحويل المورفين غير الشرعي إلى فئة كيتونات هيدرومورفين أو أحد المشتقات الأخرى مثل ثنائي هيدرومورفين (بارامورفين) والديسومورفين (بيرمونيد) والميتوبون وغيرها وتحويل الكودين إلى هيدروكودون (ديكوديد) وثنائي هيدروكودين (باراكودين) وغيرها إلى خبرة أكبر وأنواع وكميات مختلفة من المواد الكيميائية والتجهيزات التي يصعب تأمينها، وهذا ما يجعل استخدامها أندر في الأوجه غير الشرعية (رغم الإبلاغ عن بعض هذه الحالات).
التاريخ
يعود تاريخ ظهور إكسير المورفين إلى خيمياء العصور البيزنطية، لكن الصيغة الدقيقة ضاعت خلال الغزو العثماني للقسطنطينية (إسطنبول). نحو عام 1522، ذكر باراسيلسوس إكسيرًا مورفينيًا أُطلق عليه «laudanum صبغة الأفيون» من الكلمة اللاتينية laudāre التي تعني «المديح»، ووصفه بمسكن الألم القوي، لكنه أوصى باستخدامه باعتدال. تختلف الوصفة التي أعطاها جوهريًا عن صبغة الأفيون الحالية.[26]
كان المورفين أول أشباه القلويات الفعالة المكتشفة المستخلصة من خشخاش الأفيون في ديسمبر من عام 1804 في مدينة بادربورن على يدي الصيدلي الألماني فريدريك سيرتونر. في عام 1817، أشار سيرتونر إلى تجاربه التي اختبر فيها المورفين على جسده مع ثلاثة أطفال وثلاثة كلاب وفأر، والتي بلغ فيها الأشخاص الأربعة حافة الموت. أطلق سيرتونر اسم مورفيوم morphium على المادة الدوائية تيمنًا بإله الأحلام اليوناني مورفيوس كونه يزيد الرغبة في النوم. كان المورفيوم الذي صنعه سيرتونر أقوى بست مرات من الأفيون العادي، وافترض أن الجرعة الصغيرة اللازمة لإحداث تأثيراته تجعله أقل تسببًا بالإدمان، لكنه أصبح مدمنًا على الدواء، وحذر قائلًا إنه يعتبر من واجبه التنبيه إلى التأثيرات الرهيبة لمادته الجديدة «المورفيوم» سعيًا لتجنب المصائب التي يحدثها.[27]
أدخلت شركة «سيرتونر آند كومباني» الدواء إلى الأسواق العامة لأول مرة عام 1817 ليُصنف ضمن مسكنات الألم وعلاجات إدمان الأفيون والكحول. استخدم المورفين سمًا لأول مرة عام 1822 على يدي الطبيب الفرنسي إدمي كاستنغ الذي أدين بقتل أحد المرضى. بدأ الإنتاج التجاري للمورفين في مدينة دارمشتات في ألمانيا عام 1827 في الصيدلية التي شكلت نواة شركة ميرك للصناعات الدوائية، وشكلت مبيعات المورفين جزءًا كبيرًا من النمو الاقتصادي الباكر للشركة.[28]
في خمسينيات القرن التاسع عشر، أبلغ الطبيب ألكسندر وود عن تجربة حقن فيها المورفين في جسد زوجته ريبيكا، وانتشرت الإشاعات حول موتها نتيجة التثبيط التنفسي الناجم عن هذا الاختبار، لكنها عاشت عشرة أعوام بعد وفاة زوجها. اكتشف لاحقًا أن المورفين يتفوق في إحداث الإدمان على الكحول والأفيون، ونتج عن استخدامه المفرط خلال الحرب الأهلية الأمريكية ما يزيد عن 400,000 حالة من «داء الجنود» الناجم عن الإدمان على المورفينات. كانت هذه الفكرة موضع جدل بسبب ادعاء البعض أن هذا المرض مجرد كذبة ملفقة. يعود أول استخدام موثق لمصطلح «داء الجنود» إلى عام 1915.[29]
اصطنع دي أسيتيل مورفين (الذي يُعرف عادةً بالهيروين) من المورفين عام 1874، وأدخلته شركة باير إلى السوق عام 1898. تزيد فعالية الهيروين على المورفين بمقدار مرة ونصف إلى مرتين إذا أعطيا بنفس الجرعة. يستطيع الهيروين عبور الحاجز الدموي الدماغي أسرع من المورفين لقدرته على الانحلال في الشحوم، وبالتالي تزيد قدرته على إحداث الإدمان. قدرت إحدى الدراسات التي استخدمت أساليب موضوعيةً وذاتيةً متنوعةً أن نسبة فعالية الهيروين إلى المورفين المعطى وريديًا عند معادي التأهيل بعد الإدمان تبلغ 1.80-2.66 مغ من سلفات المورفين إلى 1 مغ من الهيروين (هيدروكلوريد ديامورفين).[30]
أصبح المورفين من المواد الخاضعة للرقابة في الولايات المتحدة تحت قانون هاريسون لضرائب المخدرات عام 1914، وأصبحت حيازته دون وصفة طبية جريمةً جنائيةً. كان المورفين أشيع المخدرات المسببة للإدمان في العالم حتى أزاحه الهيروين بعد اصطناعه ودخوله الاستخام السريري.
في العموم، لم تظهر أدوية فعالةً بمقدار الأفيون والمورفين والهيروين حتى اصطناع ثنائي هيدرومورفين (قرابة عام 1900) وفئة ثنائي هيدرومورفينون من الأفيونات (في عشرينيات القرن العشرين) والأوكسيكودون (1916) والأدوية المشابهة لها، بينما تأخر اصطناع بعض التركيبات الدوائية عدة سنوات (اخترع البيثيدين عام 1937 في ألمانيا). كانت المناهضات الأفيونية من بين المركبات شبه الاصطناعية نظائر ومشتقات من الكودين مثل ثنائي هيدروكودين (باراكودين) وإيثيل مورفين (ديونين) وبنزيل مورفين (بيرونين).
حتى الوقت الحاضر، ما يزال المورفين أكثر المخدرات الموصوفة التي يسعى خلفها مدمنو الأفيونات عند عدم توافر الهيروين، وقد يحتل الهيدرومورفين والأوكسيمورفين والجرعات العالية من الأوكسيكودون والميثادون وديكستروموراميد في حالات معينة أعلى القائمة في حال ثبات الشروط الأخرى استنادًا إلى الظروف المحلية وتفضيلات المستخدمين، كما حدث في أستراليا في سبعينيات القرن العشرين.[31]
يُعد الكودين الدواء المفضل في فترة التوقف عن التعاطي عند أغلب مدمني الهيروين، لكن بعضهم يستخدم ثنائي هيدروكودين ومشتقات قش الخشخاش مثل قرون الخشخاش وشاي بذور الخشخاش والبروبوكسيفين والترامادول.
تمكن روبرت روبنسون من تحديد الصيغة البنيوية للمورفين عام 1925، وحظيت ثلاثة طرق لاصطناع المورفين الكلي على الأقل على براءة اختراع بدءًا من مواد التصنيع مثل قطران الفحم وتقطير النفط. أعلن الكيميائي مارشال د. جيتس عن أولاها في جامعة روتشستر عام 1952، لكن أغلب المورفينات تُشتق من خشخاش الأفيون عبر الطريقة التقليدية أو جمع العصارة من قرون الخشخاس المحززة قبل نضجها أو عمليات المعالجة التي تعتمد على قش الخشخاش والقرون والجذوع المجففة للنبتة، وأشيع الطرق انتشارًا بينها ظهرت في هنغاريا عام 1930 على يدي عالم الأدوية الهنغاري جانوس كاباي.
اكتُشف أن المورفين يُصطنع طبيعيًا في الجسم البشري عام 2003، وكان هذا الافتراض خاضعًا للتكهنات طيلة 30 عامًا لأن العلماء وجدوا مستقبلًا في النسج البشرية يبدو أنه يتفاعل مع المورفين فقط، وأطلقوا عليه مستقبل الأفيون ميو 3. وُجد أن الخلايا البشرية المتشكلة استجابةً لورم الخلايا البدائية العصبية السرطاني تحوي آثارًا من المورفين داخلي المنشأ.
انظر أيضًا
مراجع
- ^ Bonewit-West K، Hunt SA، Applegate E (2012). Today's Medical Assistant: Clinical and Administrative Procedures. Elsevier Health Sciences. ص. 571. ISBN:9781455701506. مؤرشف من الأصل في 2023-01-10. اطلع عليه بتاريخ 2019-08-20.
- ^ Jonsson T, Christensen CB, Jordening H, Frølund C (أبريل 1988). "The bioavailability of rectally administered morphine". Pharmacol. Toxicol. ج. 62 ع. 4: 203–5. DOI:10.1111/j.1600-0773.1988.tb01872.x. PMID:3387374.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ أ ب ت ث ج "Morphine sulfate". The American Society of Health-System Pharmacists. مؤرشف من الأصل في 2018-06-12. اطلع عليه بتاريخ 2015-06-01.
- ^ Rockwood، Charles A. (2009). Rockwood and Wilkins' fractures in children (ط. 7th). Philadelphia, Pa.: Lippincott Williams & Wilkins. ص. 54. ISBN:9781582557847. مؤرشف من الأصل في 2018-06-12.
- ^ أ ب ت Courtwright، David T. (2009). Forces of habit drugs and the making of the modern world (ط. 1). Cambridge, Mass.: Harvard University Press. ص. 36–37. ISBN:9780674029903. مؤرشف من الأصل في 2019-12-17.
- ^ http://www.alshabab.gov.eg/DRUGS/pages/pages/drugs_classification/nobza%20morphin%20sound.htm نسخة محفوظة 2020-06-04 على موقع واي باك مشين.
- ^ Luch A، المحرر (2009). Molecular, clinical and environmental toxicology. Springer. ص. 20. ISBN:3-7643-8335-6. مؤرشف من الأصل في 2020-03-08.
{{استشهاد بكتاب}}:|archive-date=/|archive-url=timestamp mismatch (مساعدة) - ^ أ ب Clayton J. Mosher (2013). Drugs and Drug Policy: The Control of Consciousness Alteration. SAGE Publications. ص. 123. ISBN:9781483321882. مؤرشف من الأصل في 2019-06-12.
- ^ Fisher، Gary L. (2009). Encyclopedia of substance abuse prevention, treatment, & recovery. Los Angeles: SAGE. ص. 564. ISBN:9781452266015. مؤرشف من الأصل في 2019-06-09.
- ^ Narcotic Drugs Estimated World Requirements for 2008, Statistics for 2006. New York: United Nations Pubns. 2008. ص. 77. ISBN:9789210481199. مؤرشف من الأصل في 4 يونيو 2019. اطلع عليه بتاريخ أغسطس 2020.
{{استشهاد بكتاب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - ^ أ ب ت ث Narcotic Drugs 2014 (PDF). INTERNATIONAL NARCOTICS CONTROL BOARD. 2015. ص. 21, 30. ISBN:9789210481571. مؤرشف من الأصل (pdf) في 2018-09-16.
- ^ أ ب Triggle، David J. (2006). Morphine. New York: Chelsea House Publishers. ص. 20–21. ISBN:9781438102115. مؤرشف من الأصل في 2019-06-09.
- ^ Karch، Steven B. (2006). Drug abuse handbook (ط. 2nd). Boca Raton: CRC/Taylor & Francis. ص. 7–8. ISBN:9781420003468. مؤرشف من الأصل في 2019-06-13.
- ^ Macpherson، edited by Gordon (2002). Black's medical dictionary (ط. 40th). London: A & C Black. ص. 162. ISBN:9780713654424. مؤرشف من الأصل في 2019-12-17.
{{استشهاد بكتاب}}:|الأول1=باسم عام (مساعدة) - ^ Davis's Canadian Drug Guide for Nurses. F.A. Davis. 2014. ص. 1409. ISBN:9780803640863. مؤرشف من الأصل في 2019-12-17.
- ^ "WHO Model List of Essential Medicines" (PDF). World Health Organization. أكتوبر 2013. مؤرشف من الأصل (PDF) في 2017-08-28. اطلع عليه بتاريخ 2014-04-22.
- ^ أ ب "Morphine Sulfate". The American Society of Health-System Pharmacists. مؤرشف من الأصل في 2018-06-12. اطلع عليه بتاريخ 2011-04-03.
- ^ Meine TJ, Roe MT, Chen AY, Patel MR, Washam JB, Ohman EM, Peacock WF, Pollack CV, Gibler WB, Peterson ED (يونيو 2005). "Association of intravenous morphine use and outcomes in acute coronary syndromes: results from the CRUSADE Quality Improvement Initiative". Am. Heart J. ج. 149 ع. 6: 1043–9. DOI:10.1016/j.ahj.2005.02.010. PMID:15976786.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Sosnowski MA. "BestBets: Does the application of opiates, during an attack of Acute Cardiogenic Pulmonary Oedma, reduce patients' mortality and morbidity?". BestBets. Best Evidence Topics. مؤرشف من الأصل في 2018-09-08. اطلع عليه بتاريخ 2008-12-06.
- ^ http://www.asharqalawsat.com/details.asp?section=14&article=297771&issueno=9657 نسخة محفوظة 2020-06-04 على موقع واي باك مشين.
- ^ Thompson DR (أبريل 2001). "Narcotic analgesic effects on the sphincter of Oddi: a review of the data and therapeutic implications in treating pancreatitis". Am. J. Gastroenterol. ج. 96 ع. 4: 1266–72. DOI:10.1111/j.1572-0241.2001.03536.x. PMID:11316181.
- ^ Stefano GB, Zhu W, Cadet P, Bilfinger TV, Mantione K (مارس 2004). "Morphine enhances nitric oxide release in the mammalian gastrointestinal tract via the micro(3) opiate receptor subtype: a hormonal role for endogenous morphine". J. Physiol. Pharmacol. ج. 55 ع. 1 Pt 2: 279–88. PMID:15082884.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Calignano A, Moncada S, Di Rosa M (ديسمبر 1991). "Endogenous nitric oxide modulates morphine-induced constipation". Biochem. Biophys. Res. Commun. ج. 181 ع. 2: 889–93. DOI:10.1016/0006-291X(91)91274-G. PMID:1755865.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ "Narcotics (Opioids) | DEA". www.dea.gov. مؤرشف من الأصل في 2022-01-20. اطلع عليه بتاريخ 2021-01-21.
- ^ Crews JC، Denson DD (ديسمبر 1990). "Recovery of morphine from a controlled-release preparation. A source of opioid abuse". Cancer. ج. 66 ع. 12: 2642–4. DOI:10.1002/1097-0142(19901215)66:12<2642::AID-CNCR2820661229>3.0.CO;2-B. PMID:2249204.
- ^ Sigerist HE (1941). "Laudanum in the Works of Paracelsus" (PDF). Bull. Hist. Med. ج. 9: 530–544. مؤرشف من الأصل (PDF) في 2022-03-02. اطلع عليه بتاريخ 2018-09-05.
- ^ Offit P (مارس–أبريل 2017). "God's Own Medicine". سكيبتيكال إنكوايرر. ج. 41 ع. 2: 44.
- ^ Annual Register. J. Dodsley. 1824. ص. 1. مؤرشف من الأصل في 24 فبراير 2021. اطلع عليه بتاريخ 1 سبتمبر 2015.
Edme.
- ^ "Opiate Narcotics". The Report of the Canadian Government Commission of Inquiry into the Non-Medical Use of Drugs. Canadian Government Commission. مؤرشف من الأصل في 4 أبريل 2007.
- ^ Martin WR، Fraser HF (سبتمبر 1961). "A comparative study of physiological and subjective effects of heroin and morphine administered intravenously in postaddicts". The Journal of Pharmacology and Experimental Therapeutics. ج. 133: 388–99. PMID:13767429.
- ^ Gulland JM، Robinson R (1925). "Constitution of codeine and thebaine". Memoirs and Proceedings of the Literary and Philosophical Society of Manchester. ج. 69: 79–86.
| مورفين في المشاريع الشقيقة: | |
| أدوية أفيونية تحرير |
|---|
|
{ألفينتانيل} {بوبرينورفين} {كارفينتانيل} {كودين} {كودينون} {ديكستروبروبكسيفين} {ديامورفين (هيروين)} {ديهيدروكودئين} {فينتانيل} {هيدروكودون} {هيدرومورفون} {ميثادون} {مورفين} {مورفينون} {نالبوفين} {أوكسيكودون} {أوكسيمورفون} {بنتازوسين} {بيثيدين (ميبيريدين)} {بروبوكسيفين} {ريميفينتانيل} {سوفينتانيل} {ترامادول} |
- مورفين
- ناهضات مستقبل الأفيونيد كابا
- أدوية أساسية حسب منظمة الصحة العالمية
- أفيونيات
- أيضات ثانوية
- العلم في 1804
- إيثرات
- سموم نباتية
- شبه قلويات أفيونية طبيعية
- فينولات
- مئيضات بشرية
- مسببات الابتهاج
- معدلات تفارغية سلبية لمستقبل غابا أ
- مناهضات مستقبل الغلايسين
- مواد كيميائية تستخدم في طب الطوارئ
- مورفينانات
- ناهضات ميو-أفيونية